室温下,将0.05mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质,有关结论正确的是
| |
加入的物质 |
结论 |
| A |
50mL 1mol·L-1H2SO4 |
反应结束后,c(Na+)=c(SO42-) |
| B |
0.05molCaO |
溶液中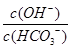 增大 增大 |
| C |
50mL H2O |
由水电离出的c(H+)·c(OH-)不变 |
| D |
0.1molNaHSO4固体 |
反应完全后,溶液pH减小,c(Na+)不变 |
用右图所示装置进行如下实验,能达到实验目的的是
| A.瓶中盛满水,从B口进气,用排水法收集NO2 |
| B.瓶中盛适量浓硫酸,从A口进气来干燥NH3 |
| C.从B口进气,用排空气法收集CO2 |
| D.瓶中装满水,A口连导管并伸入量筒中,从B口进气,用排水法测量生成H2的体积 |
分析推理是化学学习方法之一。下列实验推理中,正确的是
| A.灼热的铂丝与NH3、O2混合气接触,铂丝保持红热,说明氨的氧化反应是放热反应 |
| B.某雨水的pH小于5.6,说明雨水中一定溶解了SO2 |
C.某溶液中加入氯化钡溶液,生成白色沉淀,说明原溶液中一定含有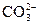 |
| D.将镁条和铝片用导线连接再插进稀NaOH溶液,镁条上产生气泡,说明镁比铝活泼 |
下表中a、b、c表示相应仪器中加入的试剂,可用右图装置制取、净化、收集的气体是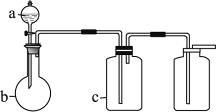
| 编号 |
气体 |
a |
b |
c |
| A |
NH3 |
浓氨水 |
生石灰 |
碱石灰 |
| B |
CO2 |
盐酸 |
碳酸钙 |
饱和NaHCO3 |
| C |
NO |
稀HNO3 |
铜屑 |
H2O |
| D |
NO2 |
浓HNO3 |
铜屑 |
NaOH溶液 |
已知:为使Fe3+、Fe2+、Zn2+较完全的形成氢氧化物沉淀,溶液的pH应分别为3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量Fe3+、Fe2+,为除去这些离子制得纯净的硫酸锌,应加入的试剂是
| A.NaOH溶液 |
| B.氨水 |
| C.KMnO4、ZnCO3 |
| D.H2O2、ZnO |
某酸性溶液中可能含有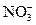 、I-、Cl-、Fe3+中的一种或几种离子,向其中加入溴水,溴水褪色,下列推测不正确的是
、I-、Cl-、Fe3+中的一种或几种离子,向其中加入溴水,溴水褪色,下列推测不正确的是
| A.一定含I- |
| B.不含Fe3+ |
| C.一定含Cl- |
D.不含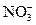 |