物质A~E均含同种元素,都是中学化学中常见的物质,它们可发生如图所表示的反应。已知A是一种淡黄色的固体,B是银白色金属单质。
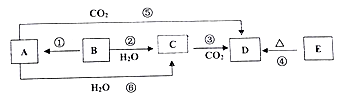
(1)反应⑤可用于潜水艇中制取氧气,相关的化学方程式为:_________,氧化剂是________,还原剂是__________;
(2)根据反应②相关的现象,从表格下方找出相应性质序号填在表格中,并在对应的位置写上该反应的化学方程式。
| |
现象 |
单质B的相关性质(填序号) |
相关的化学方程式 |
| I |
单质B浮在水面上 |
|
|
| II |
熔成一个小球 |
|
|
| III |
四处游动,发出嘶嘶的声音 |
|
|
| IV |
滴入酚酞试剂,溶液变红 |
|
与反应现象相应的性质:①反应后生成了酸性物质;②反应后生成了碱性物质;③单质B的熔点低;④单质B的密度比水的小;⑤生成了气体;⑥单质B的密度比水的密度大;
(3)D和E分别与等浓度的盐酸反应,相同条件下生成等体积的气体,则以下说法正确的是:
________(填序号)
①消耗D的质量较多;②消耗E的质量较多;③D消耗盐酸的体积更大 ④E消耗盐酸的体积更大
已知氧化性Fe3+>Cu2+>Fe2+。现有一包铁粉和铜粉混合粉末,某研究小组同学为了确定其组成,利用1.2mol/L的FeCl3溶液(其他用品略),与混合粉末反应,实验结果如下(假定反应前后溶液体积不变):
| 组别 |
||||
| V[FeCl3(aq)]/mL |
50 |
50 |
50 |
50 |
| 混合粉末质量/g |
1.2 |
2.4 |
3.6. |
4.8 |
| 反应后剩余固体质量/g |
0 |
0.64 |
1.92 |
3.12 |
分析表中数据,下列结论正确的是
A.第①组反应后溶液中剩余c(Fe3+)=0.4mol/L B.第②、③组剩余固体全是铜
C.第④组的滤液中c(Fe2+)=2.0mol/LD.原混合粉末中n(Fe)∶n(Cu)=1∶2
亚硫酸钠中有+4价的硫,它既有氧化性又有还原性。现有试剂:溴水、硫化钠溶液
亚硫酸钠溶液、稀硫酸、烧碱溶液、氨水。
①要证明Na2SO3具有还原性,应选用的试剂有
现象是
②要证明Na2SO3具有氧化性,应选用的试剂有、稀硫酸。
现象是
写出该反应的离子方程式:
除去括号中的杂质,将操作方法和化学方程式填入表中空格。
| 操作方法 |
化学方程式 |
|
| ①SiO2(CaCO3) |
||
| ② Fe(Al) |
||
| ③ SO2 (HCl) |
在一定条件下可实现下图所示物质之间的 变化
变化
请填写以下空白:
(1)孔雀石的主要成份是CuCO3·Cu(OH)2(碱式碳酸铜)受热易分解。 上图中的F是
上图中的F是
(2)写出明矾溶液与过量的NaOH溶液反应的离子方程式
(3)图中所得G和D都为固体混合后在高温下可发生反应写出该反应化学方程式
(4)每生成1mol D同时生成mol E。
由于空气中,按体积计算,氧气约占,所以硫在空气中燃烧,发出色火焰,而在纯氧中燃烧,则发出色火焰。生成的气体叫做,具有气味。