Ⅰ.图1是某压强下工业合成氨生产过程中,N2与H2按体积比为1:3投料时,反应混合物中氨的体积分数随温度的变化曲线,其中一条是经过一定时间反应后的曲线,另一条是平衡时的曲线。
(1)图中表示该反应的平衡曲线的是__________(填“Ⅰ”或“Ⅱ”);由图中曲线变化趋势可推知工业合成氨的反应是___________(填“吸热”或“放热”)反应。
(2)图中a点,容器内气体n(N2):n(NH3)= ____________,图中b点,v(正)_________v(逆)(填“>”、“=”或“<”)。
Ⅱ.以工业合成氨为原料,进一步合成尿素的反应原理为:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g)
CO(NH2)2(l)+H2O(g)
工业生产时,需要原料气带有水蒸汽,图2中曲线I、Ⅱ、Ⅲ表示在不同水碳比[n(H2O)/n(CO2)]时,CO2的转化率与氨碳比[n(NH3)/n(CO2)]之间的关系。
(1)写出该反应的化学平衡常数表达式____________________
(2)曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是_________,判断依据是_______________
(3)测得B点氨的转化率为40%,则x1=__________。
17gNH3共有 mol氢原子,0.1molH2S共有约 个原子,同温同压下,同体积的NH3和H2S气体的质量比为 ;同温同压下,同质量的NH3和H2S气体的体积比为
在H、O、C、Na四种元素中,选择适当的元素组成符合下列要求的物质,将它们的化学式填写在以下空格中。
| 酸性氧化物 |
碱性氧化物 |
酸 |
碱 |
正盐 |
酸式盐 |
某学生利用下面实验装置探究盐桥式原电池的工作原理。按照实验步骤依次回答下列问题:
(1)导线中电子流向为__________(用a、b表示)。
(2)写出装置中锌电极上的电极反应式:_______________;
(3)若装置中铜电极的质量增加0.64 g,则导线中转移的电子数目为_____;(用“NA”表示)
(4)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,对盐桥中的K+、Cl-的移动方向的表述正确的是________。
| A.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动 |
| B.盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动 |
| C.盐桥中的K+、Cl-都向左侧烧杯移动 |
| D.盐桥中的K+、Cl-几乎都不移动 |
(5)实验室用惰性电极电解200ml的硝酸银溶液一段时间后,撤去电源,若加入23.2g氧化银恰好使电解液恢复到原来状态,则电解过程中转移电子数为 mol;若加入25.0g氢氧化银恰好使电解液恢复到原来状态,则原硝酸银溶液的物质的量浓度为 mol·L-1。
化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热量的形式表现出来,叫做反应热。由于反应的情况不同,反应热可分为许多种,如标准燃烧热和中和反应反应热等。
(1)下列ΔH表示物质标准燃烧热的是________;表示中和反应反应热的是________。(填“ΔH1”、“ΔH2”、“ΔH3”等)
A.2H2(g)+O2(g)===2H2O(l) ΔH1
B.C(s)+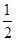 O2(g)===CO(g)ΔH2=-Q1kJ·mol-1
O2(g)===CO(g)ΔH2=-Q1kJ·mol-1
C.CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH3
D.C(s)+O2(g)===CO2(g)ΔH4=-Q2kJ·mol-1
E.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH5
(2)2.00 g C2H2气体完全燃烧生成液态水和CO2气体,放出99.6 kJ的热量,写出该反应的热化学方程式:_________________。
(3)根据题(1)中B、D判断1 molCO(g)完全燃烧的ΔH= 。
(4)反应E的ΔH6可以用如图所示的装置进行测量。实验中直接测定的数据是 ;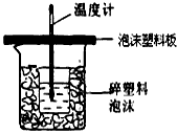
从实验装置上看,图中尚缺少的一种玻璃用品是_____________;大烧杯上如不盖硬纸板,求得的中和反应的反应热的数值________(填“偏大”“偏小”或“无影响”)。
(1)反应N2O4(g) 2NO2(g);DH>0的平衡体系中,在298K时,平衡常数为K1,在273K时,平衡常数为K2,在373K时平衡常数为K3,K1、K2、K3之间的数量大小关系是 。
2NO2(g);DH>0的平衡体系中,在298K时,平衡常数为K1,在273K时,平衡常数为K2,在373K时平衡常数为K3,K1、K2、K3之间的数量大小关系是 。
(2)在298K时,将0.40 mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间/s n/mol |
0 |
20 |
40 |
60 |
80 |
100 |
| n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
| n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
20~40 s内用N2O4表示的平均反应速率为________mol·L-1·s-1;298K时该反应的平衡转化率=________;反应进行至100 s后将反应混合物的温度降低,混合气体的颜色________(填“变浅”、“变深”或“不变”);
(3)298K时,反应2NO2(g) N2O4(g);DH<0达到平衡后,根据下列图像判断引起平衡移动的因素及平衡移动的的方向:
N2O4(g);DH<0达到平衡后,根据下列图像判断引起平衡移动的因素及平衡移动的的方向:
图(2)平衡将向_______方向移动;图(3)引起平衡移动的因素是_____________,图(4)引起平衡移动的因素是______________。