市售一次电池品种很多,碱性锌锰电池在日常生活中用量很大。回收废旧锌锰电池并进行重新处理,可以获得MnO2及其他副产品,其工艺流程如下:
已知:“锰粉”的主要成分有MnO2、Zn(OH)2、MnOOH、碳粉,还含有少量铁盐和亚铁盐。常温下,生成氢氧化物沉淀的pH如下表:
| 物质 |
Fe(OH)3 |
Fe(OH)2 |
Zn(OH)2 |
Mn(OH)2 / Mn(OH)3 |
| 开始沉淀pH |
2.7 |
7.6 |
5.7 |
8.3 |
| 完全沉淀pH(c≤1.0×10-5mol/L) |
3.7 |
9.6 |
8.0 |
8.8 |
(1)加入NaOH溶液调节pH=8.0,目的是____________________;计算常温下Zn(OH)2的溶度积常数Ksp[Zn(OH)2]=____________________。
(2)写出滤液2中的Mn2+变成MnO2的离子方程式_________________________。
(3)写出滤渣B与稀硫酸在pH=5时反应的化学方程式______________________。
(4)工艺中还可以将滤液4进行_____________、_____________、_____________、洗涤得到含结晶水的硫酸盐晶体。
(5)MnO2常用来制取KMnO4。在一定条件下将MnO2氧化为K2MnO4,然后用铁作阴极、铂作阳极电解K2MnO4溶液得到KMnO4。电解K2MnO4溶液的总反应方程式为______________________。
下表是元素周期表的一部分,根据所给元素,用元素符号或化学式回答下列问题。
(1)非金属性最强的元素是;
(2)Ne 原子结构示意图为;
(3)C 与N 中,原子半径较小的是;(4)氯水具有漂白作用,是由于其中含有;
(5)元素最高价氧化物对应的水化物中,碱性最强的是
 ,呈两性的是;
,呈两性的是;
(6) 镁是制造汽车、飞机、
镁是制造汽车、飞机、 火箭的重要材料。写出工业上电解熔融
火箭的重要材料。写出工业上电解熔融
氯化镁获得金属镁的化学方程式。
我国政府十分关注学生营养状况,把每年5月20日确定为“中国学生营养日”。右表为南方某山区学校食堂午餐的食谱。
请用所学知识填写空格:
(1)食谱中的米饭主要含(填“淀粉”或“纤维素”);
(2)从营养均衡及学生身体发育需要的角度考虑,你认为以上食谱中应增 加富含蛋白质的食物是(只填一种);
加富含蛋白质的食物是(只填一种);
(3)在我国北方,学生更多以面食为主,而NaHCO3是制作面食的常用疏松剂,写出NaHCO3受热分解的化学方程式________________;
(4)营养失衡可能导致胃病,而NaHCO3 是可用作治疗胃酸(主要含盐酸)过多的药剂,写出该反应的离子方程式。
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,
其余为氧。A的相关反应如下图所示:
已知R-CH=CHOH(烯醇)不稳定,很快转化为R-CH2CHO。根据以上信息回答下列问题:
(1)A的分子式为 ;
(2)反应②的化学方程式是 :
(3)A的结构简式是 ;
(4)反应①的化学方程式是 。
(5)A有多种同分异构体,写出四个同时满足:
(i)能发生水解反应;
(ii)能使溴的四氯化碳溶液褪色两个条件的同分异构体的结构简式:
、 、
、 ;
(6)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为。
按要求完成下列各题:
(1)写出乙醛与氢气反应的化学方程式:
。
(2)正丙醇催化氧化反应的化学方程式:
。
(3)丙醛和新制备的银氨溶液的反应:
 。
。
(7分)已知: A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平的标志。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。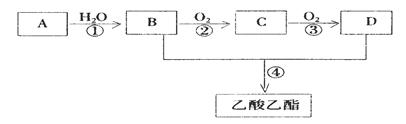
回答下列问题:
(1)B、D分子中官能团名称分别是 、 。
(2)写出下列反应的反应类型:① 反应,
②  反应,④ 反应。
反应,④ 反应。
(3)写出下列反应的化学方程式:
③ ;④
;④