下列由相关实验现象所推出的结论正确的是
| A.向某溶液中加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,则该溶液一定含有SO42- |
| B.向某溶液中加入CCl4,CCl4层显紫色,证明原溶液中存在I2 |
| C.向某溶液中加入稀盐酸,产生的气体能使澄清石灰水变浑浊,则溶液中一定含有CO32- |
| D.向一定浓度的Na2SiO3溶液中通入适量CO2气体,出现白色沉淀,说明H2SiO3的酸性强于H2CO3 |
化学与生活密切相关,下列说法不正确的是()
| A.风能、生物质能、沼气是可再生能源,煤、石油、天然气是不可再生能源 |
| B.“84消毒液”具有强氧化性,可做环境的消毒剂从而预防流感 |
| C.雾霾天气严重影响人类健康,PM2.5是指大气中直径小于或者等于2.5微米的颗粒物,也称为“细颗粒物”PM2.5在空气中可能形成胶体。 |
| D.已知水热反应是指在高温高压下,将二氧化碳转化为有机物的技术,可以降低自然界中碳的含量 |
有五瓶失去标签的无色溶液A,B,C,D,E分别为氢氧化钠溶液、硫酸钠溶液、硝酸钠溶液、氯化钠溶液和碳酸钠溶液。为把它们一一鉴别开,按下面的实验步骤进行:
(1)分别取五种溶液少许,加入无色试剂X,A、B、E三种溶液无变化,C、D溶液中有白色沉淀生成。
(2)分别另取五种溶液少许,加入无色酚酞试液,A、B、C三种溶液无变化,D、E两种溶液显红色。
(3)分别另取五种溶液少许,加入无色试剂Y,A、B、C、E四种溶液均无变化,D溶液中有气泡生成。
(4)分别取A、B两种溶液,各滴入AgNO3溶液,A中有白色沉淀生成。
回答下列问题:①确定A、B、C、D、E各是什么溶液。
A为_______溶液,B为________溶液,C为_________溶液,D为_________溶液,E为_______溶液
②所加试剂X、Y各是什么溶液。试剂X为___________溶液,试剂Y为___________溶液
有Na2CO3、AgNO3、BaCl2 、HCl及NH4NO3五瓶无标签的溶液,为鉴别它们,取四支试管分别装入一种溶液,再向上边四支试管中加入少许剩下的一种溶液,则下列表述错误的是()
| A.若三支试管出现沉淀时,则后加入的是AgNO3 |
| B.全部没有什么现象变化时,则后加入的是NH4NO3 |
| C.一支试管出现气体,另两支试管出现沉淀时,最后加入的盐酸 |
| D.若只有两支试管出现沉淀时,则后加入的是BaCl2溶液 |
将标准状况下的V LHCl(气)溶于1000g水中,得到的盐酸密度为rg/cm3,则该盐酸的物质的量浓度为()
A.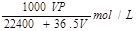 |
B. |
C. |
D.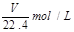 |
某氯原子的质量为a g,12C原子的质量为b g,用NA表示阿伏加德罗常数的值,下列说法中不正确的是()
| A.y g该氯原子所含的电子数为17y/a |
| B.x g该氯原子的物质的量一定是x/(a × NA)mol |
| C.1mol该氯原子的质量是aNA g |
| D.该氯原子的摩尔质量为a g/mol |