2015 年,中国药学家屠呦呦获得诺贝尔生理学或医学奖,其突出贡献是创制新型抗疟药青蒿素和双氢青蒿素.已知青蒿素的结构如图所示,有关青蒿素的说法,不正确的是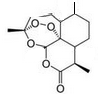
| A.分子式为C15H22O5 |
| B.能够发生水解反应 |
| C.每个分子中含有4个六元环 |
| D.青蒿素能够治疗疟疾可能与结构中存在过氧键基团有关 |
铅蓄电池的工作原理为:Pb+PbO2+2H2SO4===2PbSO4+2H2O,研读下图,下列判断不正确的是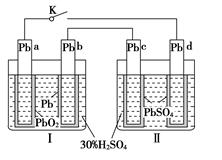
| A.K闭合时,d电极反应式:PbSO4+2H2O-2e-===PbO2+4H++SO42- |
| B.当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为 0.2 mol |
| C.K闭合时,Ⅱ中SO42-向c电极迁移 |
| D.K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极 |
甲、乙两个电解池均以Pt为电极,且互相串联,甲池盛有AgNO3溶液,乙池中盛有一定量的某盐溶液,通电一段时间后,测得甲池中电极质量增加2.16 g,乙池中电极上析出0.24 g 金属,则乙池中溶质可能是
| A.CuSO4 | B.MgSO4 | C.Al(NO3)3 | D.Na2SO4 |
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O= Fe(OH)2+2Ni(OH)2。下列有关该电池的说法不正确的是
| A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
| B.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
| C.电池充电过程中,阴极附近溶液的pH降低 |
| D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O |
如图所示是298 K时N2与H2反应过程中,能量变化的曲线图.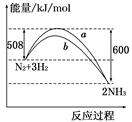
下列叙述正确的是
A.该反应的热化学方程式为:N2+3H2 2NH3 ΔH=-92 kJ/mol 2NH3 ΔH=-92 kJ/mol |
| B.a曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热改变 |
| D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1 |
反应mA(s)+nB(g) pC(g) ΔH<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,
pC(g) ΔH<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,
下列叙述中一定正确的是
| A.n>p |
| B.x点表示的正反应速率小于逆反应速率 |
| C.x点比y点时的反应速率慢 |
| D.若升高温度,该反应的平衡常数增大 |