下列离子方程式中书写正确的一组是( )
① 向明矾溶液中加入Ba(OH)2溶液至A13+ 刚好完全沉淀:
Al3++ SO42-+3OH-+Ba2+= BaSO4↓+Al (OH)3↓
② 氟气和水反应:2F2+2H2O = 4H++4F-+O2
③ 向澄清石灰水中加入少量小苏打溶液:
Ca2++OH-+HCO3- = CaCO3↓+H2O
④ 铜片投入稀HNO3溶液:Cu+NO3-+4H+ = NO↑+2H2O+Cu2+
⑤ 钠与水反应:Na +2 H2O = Na+ +OH— + H2↑
⑥ 碳酸钙放入盐酸中: CO32- + 2H+ = CO2↑ +H2O
⑦ 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
⑧ 过量氯水与FeI2溶液作用: 2Fe2+ + 2I—+ 2Cl2 =" 2" Fe3+ + I2 + 4Cl—
| A.①②③④ | B.③⑦ | C.①③④⑤ | D.①④⑥⑦⑧ |
两份等质量的铝粉,一份投入足量的稀盐酸中,另一份投入足量的氢氧化钠溶液中,则生成氢气的质量比为
| A.2:3 | B.3:2 | C.36.5:40 | D.1:1 |
除去SO2中混有的HC1气体,可选用的试剂是
| A.石灰水 | B.浓硫酸 |
| C.饱和NaHSO3溶液 | D.饱和Na2SO3溶液 |
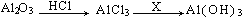 ,在以Al2O3为原料制备Al(OH)3时,X适宜用的试剂是
,在以Al2O3为原料制备Al(OH)3时,X适宜用的试剂是
| A.NH3 | B.CO2 | C.NaOH | D.HCl |
下列物质既可以通过金属与氯气反应制得,又可以通过金属与稀盐酸反应制得
| A.FeCl2 | B.FeCl3 | C.CuCl2 | D.AlCl3 |
往AlCl3溶液中逐滴滴入NaOH溶液至过量,可观察到的现象是
| A.有白色絮状沉淀产生,且不溶解 |
| B.先有白色絮状沉淀,后又溶解 |
| C.一直无明显现象 |
| D.先无现象,后有白色絮状沉淀 |