某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g).实验测得不同温度下的平衡数据列于如表:
2NH3(g)+CO2(g).实验测得不同温度下的平衡数据列于如表:
| 温度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
| 平衡总压强(kPa) |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
| 平衡气体总浓度 (×10-3mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
①可以判断该分解反应已经达到化学平衡的是___________;
A.2v(NH3)═v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时氨基甲酸铵的分解平衡常数___________;
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量___________(填“增加”、“减小”或“不变”);
④氨基甲酸铵分解反应的焓变△H______0;
(2)已知:NH2COONH4+2H2O⇌NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示.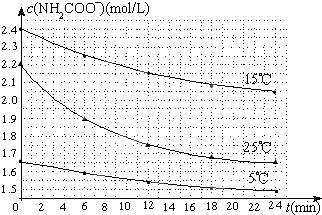
⑤计算25℃时,0~6min氨基甲酸铵水解反应的平均速率______________;
⑥根据图中信息,如何说明水解反应速率随温度升高而增大_____________________。
X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”):________________,理由是________________________________________________________________________________________________________________________。
(2)Y是________________,Z是________________,W是________________。
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8∶2∶4∶1。写出该化合物的名称及化学式____________________________________________________。
已知:A、B、C、D分别是中学化学中常见的四种不同粒子,它们之间有如下的反应关系: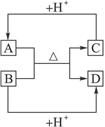
(1)如果A、B、C、D均是10电子粒子,请写出:A的化学式___________________。
(2)如果A和C是18电子的粒子,B和D是10电子粒子,请写出:
①A与B在溶液中反应的离子方程式:___________________________________________。
②根据上述离子方程式,可以判断C与B结合质子的能力大小是(用化学式或离子符号表示):___________________>___________________。
(8分)有几种元素粒子的核外电子层结构如图所示: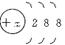
(1)某电中性粒子一般不和其他元素的原子反应,这种粒子的符号是______________。
(2)某粒子的盐溶液,能使溴水褪色,并出现浑浊,这种粒子的符号是_________________。
(3)某粒子氧化性甚弱,但得到电子后还原性很强,且这种原子有一个单电子,这种粒子的符号是______________________。
(4)某粒子还原性虽弱,但失电子后氧化性很强,且这种原子得一个电子即达稳定结构,这种粒子的符号是______________________。
A、B、C、D、E、F六种物质在一定条件下有如下图所示的相互转化关系,所有反应物和生成物均已给出,根据不同信息分别完成(1)(2)两个小题。
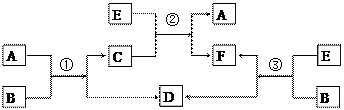 |
(1)若反应①、②、③均为水溶液中的置换反应,A、D、E为卤素单质,则A、D、E的氧化性由强到弱的顺序为 (填写相应的字母),其中A的化学式是 。
(2)若B为一种淡黄色固体,绿色植物的光合作用和呼吸作用可实现自然界中D和E的循环。反应①的化学方程式是 。在反应③中,若生成1 mol D,则转移电子的数目为 。
按下面的实验过程填空: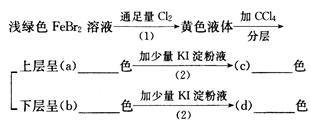
写出上述反应的化学方程式:
(1)_________________________________________________________
(2)_________________________________________________________
(3)_________________________________________________________