根据下列实验装置图,回答问题
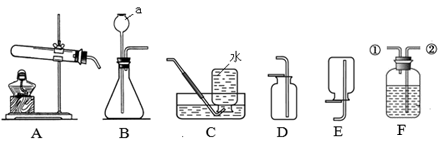
(1)写出图中仪器a的名称: 。
(2)实验室用高锰酸钾制取氧气的化学方程式为 , 可选择的发生装置为 (填字母)。
(3)实验室用石灰石和稀盐酸反应制取二氧化碳的化学方程式为 ,该反应生成的二氧化碳中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置除去氯化氢气体,则该混合气体应从F装置的 口(填“①”或“②”)通入。
(7分)A、B、C、D、E、F是初中化学中常见的物质,其中A为黑色固体,D为难溶于水的蓝色固体,F为既不溶于水也不溶于稀硝酸的白色固体,其余均为溶液,它们之间存在如下转化关系:
根据上述转化关系回答: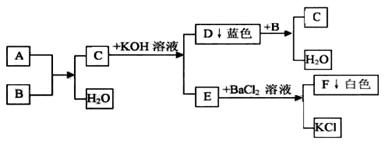
(1)写出指定物质的化学式:D;E
(2)写出上述关系中E转化成F的化学方程式,
(3)工业上通常可用A来____________________________________
(4)农业上用C物质、石灰加水配制农药波尔多液时,不能在铁制容器内配制的原因是。
(5分)生活中处处有化学。
(1)人类六大营养素中,能供给人体能量的有油脂、蛋白质和。青少年缺(填写元素符号)会患佝偻病和发育不良。
(2)下列做法有益人体健康的是。
| A.霉变的大米洗净后食用 |
| B.大量使用防腐剂,延长食品保存期 |
| C.大量出汗后,适量饮用含无机盐的饮料 |
| D.每天摄入一定量的蔬菜、水果等含维生素较多的食物 |
(3)化肥可提供农作物生长需要的营养元素,磷矿粉化学式为[Ca3 (P04)2] 属于(选填“氮”、“磷”或“钾”)肥,尿素[化学式为CO(NH2)2]中氮元素的质量分数为(计算结果保留一位小数)
下面A图是元素周期表的部分结构示意图,图B、图C是某两种元素的原子结构示意图。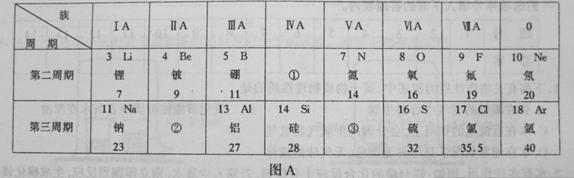
(1)原子序数为13的元素,其符号为:_______.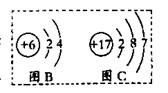
(2)图B是某元素的原子结构示意图,该元素在图中的位置是_________(选①、②或③)
(3)图C是氯元素的原子结构示意图,图A中与氯元素在同一纵行有氟元素等,氟原子结构与氯原子结构相似。由此推测,氟原子在化学反应中易(选填“得”或“失”)_________电子。氟元素若与②形成化合物的化学式为___________。
(4)试写出13号元素与8号元素形成化合物的化学反应原理______________________________
某食盐样品中含有少量沙土、氯化钙和氯化镁。以下是除去食盐样品中沙土、氯化钙和氯化镁的实验流程: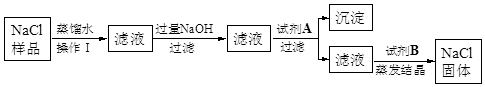
根据流程图回答:
(1)操作Ⅰ的名称是,加入的试剂A是,沉淀是;
(2)写出NaOH与杂质反应的化学方程式
(3)加入试剂B的目的是;
(4)蒸发结晶时用到玻璃棒的作用是
根据铁丝在氧气中燃烧情况,用化学用语填空:
(1)铁的化学式;
(2)铁丝燃烧的化学方程式___________
(3)试表示生成的黑色固体中金属元素的化合价:___________
(4)铁的化合物中有一种叫硫酸亚铁的物质,该物质中阴离子符号是___________