化合物A只由两种非金属元素组成,A不稳定,一定条件下爆炸生成B、C,以下为相关物质的转化关系,其中B、C、D、J为单质,其中B、D为空气的主要成分,只有J为固体,E为红棕色氧化物固体,反应①、②都是工业生产上的重要反应(部分生成物略),④反应中K过量。
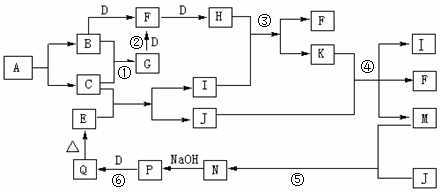
(1)写出反应②的化学反应方程式 。
(2)G的水溶液呈碱性的原因是 。
(3)标况下,将集满H气体的试管倒扣于水槽中,充分反应后所得溶液的物质的量浓度为 。
(4)P→Q反应过程中会观察到的实验现象为 。
(5)如何检验M溶液中阳离子 。
(6)M溶液在强碱性环境下可被KClO溶液氧化制得K2JO4试着写出该反应的离子方程式: 。
四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
| X |
Y |
|
| Z |
W |
请回答下列问题:
(1)元素Z位于周期表中第______________周期,___________族;
(2)XW2的电子式为_______________;
(3)Y的最高价氧化物的化学式为________________;
(4)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且W的质量分数约为70%。该化合物的化学式为_________________。
A~H及X均为中学化学常见物质,X是一种金属单质,A、B是周期表中相邻元素,且A在常温下为气体。它们在一定条件下有如下转化关系(图中条件均已略去)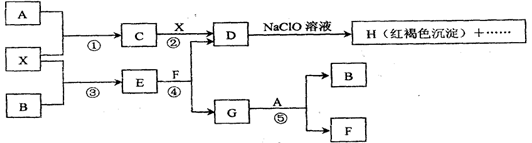
试回答下列问题:
(1)写出 C物质的化学式:。
(2)在上述①~⑤反应中肯定不属于氧化还原反应的是(填编号)。
(3)用离子方程式表示在D溶液中加入NaClO溶液产生红褐色沉淀的原因:
 。
。
(4)请写出C腐蚀铜板制印刷电路板的离子方程式: ____。
(8分)亚硝酸(HNO2)是一种比醋酸略强的弱酸,很不稳定,易发生自身氧化还原反应而分解。
(1)低温下,将等物质的量的NO和NO2通入水中,可制得HNO2,反应的化学方程式为__________________________________________________________.
(2)NO既有氧化性又有还原性,其氧化产物或还原产物与溶液的pH的关系如下表所示:
| pH范围 |
大于7 |
小于7 |
| 产物 |
NO |
NO、N2O、N2中的一种 |
①在碱性条件下,NaNO2溶液与NaClO溶液反应的离子方程式为
_________________________________________________________.
②若HNO2与氢碘酸反应时按物质的量之比1∶2进行,且I-被氧化成I2,则产物中含氮的物质为__________(填化学式).
(3)在冷冻的NaNO2溶液中加入或通入下列物质,不能制得HNO2的是________(填序号).
a.稀H2SO4 b.稀HCl c.CO2d.SO2
(4分)有一瓶澄清的溶液,其中可能含NH4+、K+、Na +、Mg2+、Ba2+、 Al3+、 Fe3+、SO42-、CO32-、NO3-、 Cl-、I-,取该溶液进行如下实验:
Cl-、I-,取该溶液进行如下实验:
⑴用pH试纸检验,表明溶液呈强酸性;
⑵取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置CCl4层呈紫红色;
⑶取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
⑷取部分上述呈碱性的溶液,加Na2CO3溶液,有白色沉淀生成;
⑸将⑶得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定并回答:在溶液中肯定存在的上述离子有 ,不能确定是否存在上述的离子有______________。
(8分) 某有机物A只含有C、H、O三种元素,常用作有机合成的中间体。现将8.4 g该有机物在14.56L(标况下)O2经充分燃烧后将产生的热气体(无有机物)先通过足量的无水CaCl2固体,发现该固体增重7.2g,然后再将该剩余气体通入足量的澄清石灰水,石灰水增重22.0g;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1。(注:—OH接在不饱和碳上为不稳定结构)
(1)通过计算确定该有机物A的分子式为, A的结构简式为。
(2)有机物B是A的同分异构体,1 mol B可与1mol Br2加成。该有机物所有碳原子在同一个平面,没有顺反异构现象。请写出B的结构简式是。