在学习过程中,小青同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体也有多种可能?
【猜 想】碳与氧化铜反应生成的气体中:①只有CO2,则发生的化学方程式是 ;
②只有 ;③既有CO,又有CO2。
【查阅资料】浸有磷钼酸溶液的氯化钯试纸遇CO2无变化,但遇到微量CO会立即变成蓝色。
【方案设计】通过上述资料和已有知识,小青初步设想用浸有磷钼酸溶液的氯化钯试纸和澄
清的石灰水对碳与氧化铜反应生成的气体进行检查。
【实验验证】经过思考之后,小青设计了如下实验装置:
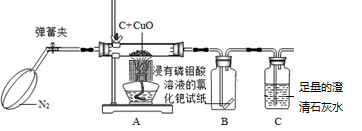
【实验步骤】
(1)打开弹簧夹,先通一会儿纯净、干燥的N2,通一会儿N2的目的是 ;
(2)关闭弹簧夹,点燃酒精灯加热。
【结 论】充分反应后,小青观察到:试纸 ,石灰水 ,证明猜想③是正确的,
A中可能观察到的现象 。
【定量计算】小青称取碳和氧化铜的混合物的质量为1g,充分反应后,装置C的质量增
加了0.22g。计算装置C中生成碳酸钙的质量是多少克?
【反思与评价】从环保的角度分析该实验装置中不完善之处是 。
某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
【查阅资料】
①生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质(不与酸反应).
②生产原理反应:NaCl+ NH3 + CO2 + H2O= NaHCO3↓+ NH4Cl,分离得晶体B,并使其充分受热,可分解制得纯碱,同时得到二氧化碳和水.
③氯化铵分解的化学方程式是NH4Cl △ NH3↑+HCl↑.
④部分生产流程如下图所示:
【问题讨论】
(1)①溶液A中的溶质有NaCl和、,
②操作Ⅱ的名称为.
③流程中Na2CO3溶液的作用是除去粗盐中的.
④写出加入NaOH溶液与MgCl2反应的化学方程式.
⑤晶体B受热分解的化学方程式为.
(2)上述生产流程中可循环使用的是(填序号).
A.NaOH B.NH3 C.HCl D.CO2
【组成探究一】
(3)设计实验检验纯碱样品中是否混有晶体B,请完成下表
| 选择的装置 |
实验现象 |
实验结论 |
| 选择的装置(填序号) |
实验现象 |
实验结论 |
| 样品不含晶体B |
【组成探究二】
(4)取纯碱样品加水溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.产生沉淀的方程式为,由此确定纯碱样品含有杂质NaCl.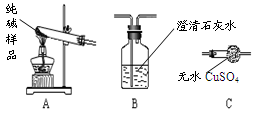
【组成探究三】
(5)同学们为了测定该纯碱样品的纯度,设计了如下实验: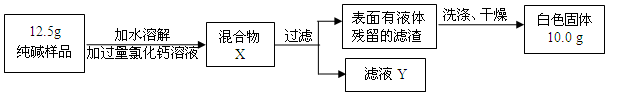
①判断加入氯化钙溶液是否过量的方法是,然后观察现象判断.
②判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加,然后观察现象判断.
A.氯化钡溶液B.硝酸银溶液 C.碳酸钠溶液 D.稀盐酸
③根据实验数据,计算样品中碳酸钠的质量分数是多少?(写出计算过程.3分)
水煤气是一种工业上常用的气体燃料,一般用焦炭和水蒸气在高温下反应制得,含有少量的CO2和水蒸气杂质。某化学兴趣小组对水煤气的主要成分进行探究。
【查阅资料】
(1)白色的无水硫酸铜粉末遇水变成蓝色;
(2)Na2CO3与少量盐酸反应生成NaHCO3和NaCl,与过量盐酸反应时生成NaCl、H2O、CO2。
【实验假设】
①可燃气体是CO;②可燃气体是H2;③可燃气体是 。
【实验过程】
实验小组按以下流程进行实验(所用试剂均为足量):
实验中,发现黑色氧化铜变红,且,证明水煤气含有H2;
还观察到澄清石灰水变浑浊,证明水煤气中含有另一可燃气体是。
【实验反思】
根据实验结论,甲同学认为实验应保证安全,防止中毒。对尾气的处理方法是。
【实验拓展】
(1)实验后,乙同学认为欲检验所用NaOH是否完全消耗,可向溶液中滴入几滴稀盐酸,若没有气体产生,则溶液中还有NaOH剩余。但丙同学认为乙同学的设计是错误的,理由是;
(2)丁同学通过本次实验,结合查阅的资料发现,不用任何其它试剂,只用试管和胶头滴管就可以鉴别稀盐酸和碳酸钠两种无色溶液。正确的鉴别方案及结论是。
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验。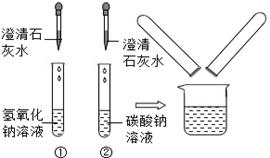
(1)写出试管②中碳酸钠与氢氧化钙反应的化学方程式:。
(2)实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究。
【提出问题】滤液中除水外还含有哪些物质?
【猜想】小红认为:只含氢氧化钠;小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;你认为还可能是(写一种猜想)。
【讨论】你认为小红、小明、小亮三位同学中谁的猜想不合理,请说明理由:。
【实验设计】设计一个简单的实验证明你的猜想正确。
| 实验步骤 |
实验现象 |
实验结论 |
| 取样于试管中, |
你的猜想正确 |
【实验分析】小亮同学针对自己的猜想进行了如下实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 取样于试管中,滴入几滴稀盐酸 |
没有气泡产生 |
自己的猜想不成立 |
你认为小亮同学对实验结果判断是否正确?请说明理由:。
【反思拓展】在分析化学反应后所得溶液中溶质的成分时,除考虑生成物外还需考虑。
在一次化学实验探究活动中,老师给某学习小组一瓶由碳酸钠溶液与澄清石灰水混合反应后,并经过滤得到的无色滤液,要求对该无色滤液中溶质的成分进行探究,请你一同参与他们的探究活动。
【提出猜想】滤液中溶质的成分有如下几种可能:
| A.NaOH |
| B.Na2CO3、Ca(OH)2、NaOH |
| C.Na2CO3和NaOH |
| D. 【讨论交流】(1)上述猜想中,肯定不成立的一项是(填猜想序号),其理由是; (2)某同学取少量溶液于试管中,滴加过量稀盐酸,发现无气泡产生,说明是不成立的(填猜想序号)。 (3)为了进一步确定溶液的成分,同学们设计实验方案,写出实验步骤以及预期现象与结论 实验步骤 预期现象及实验结论 |
(10分)人类的生产和生活都离不开金属。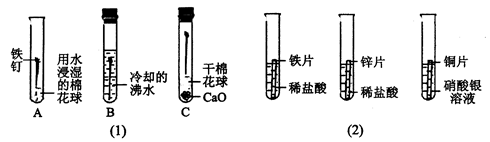
(1)在图(1)所示条件下,铁钉锈蚀最快的是试管(填序号),B装置说明铁生锈的条件是。
(2)铝的大规模开发和利用比铜和铁晚,这是因为。
(3)某研究小组的同学为探究铁、铜、锌、银的金属活动性顺序,设计如图(2)所示的三个实验(其中金属均已用砂纸打磨,且形状、大小相同;所用稀盐酸的溶质质量分数、用量也相同)。
通过观察,甲同学很快判断锌的活动性比铁强,据你分析,甲同学依据的实验现象是;
他发现铜片表面有银白色固体附着,这说明活动性Cu(填“>”“<”或“=”)Ag,反应的化学方程式是。
(4)乙同学认为上述实验不足以得出四种金属的活动性顺序,想再补充一个实验,请你和乙同学一起设计一个实验方案并进行实验,达到探究目的。
| 实验步骤 |
实验现象 |
实验结论 |