“低碳循环”引起各国的高度重视,而如何降低大气中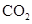 的含量及有效地开发利用
的含量及有效地开发利用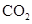 ,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题
,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
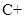
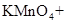
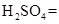
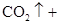
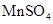 +
+ 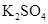 +
+ 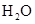
(2)将不同量的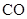 (g)和
(g)和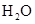 (g)分别通入到体积为 2L的恒容密闭容器中,进行反应
(g)分别通入到体积为 2L的恒容密闭容器中,进行反应
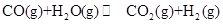 ,得到如下二组数据:
,得到如下二组数据:
| 实验组 |
温度℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
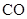 |
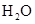 |
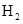 |
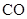 |
|||
| 1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
| 2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
①实验1中以 表示的反应速率为 (保留二位小数,下同)。
表示的反应速率为 (保留二位小数,下同)。
②实验2条件下平衡常数K=___ ___,该反应为 (填“吸”或“放”)热反应。
(3)已知在常温常压下:
①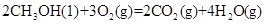
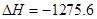 kJ/mol
kJ/mol
②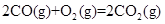
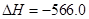 kJ/mol
kJ/mol
③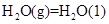
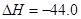 kJ/mol
kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式
(4)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。
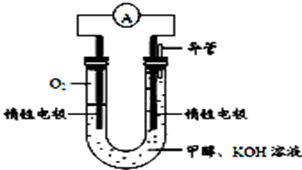
①该电池正极的电极反应为 。
②该电池工作时,溶液中的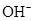 向____________极移动。
向____________极移动。
已知F为高分子化合物: 。
。
C分子结构中只含有一种氢。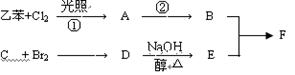
(1)写出下列物质结构简式
B:C:E:
(2)判断①②反应类型:、
(3)写出D→E的化学方程式
研究有机物一般经过以下几个基本步骤:分离、提纯 → 确定实验式 → 确定分子式 → 确定结构式。
已知:①2R-COOH + 2Na → 2R-COONa + H2 ↑
②R-COOH + NaHCO3 → R-COONa + CO2↑ + H2O
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实 验 步 骤 |
解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为。 |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g。 |
(2)A的分子式为。] |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)用结构简式表示A中含有的官能团 。 |
(4)A的核磁共振氢谱如下图: |
(4)A中含有种氢原子。 综上所述, A的结构简式为。 |
(1)请根据官能团的不同对下列有机物进行分类:
①(CH3)3CCH2OH②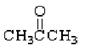 ③
③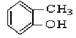
④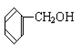 ⑤
⑤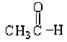 ⑥
⑥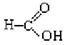
上述物质中,属于芳香醇的是,属于酚类的是属于羧酸类的是,属于醛类的是(填序号)
(2)下列属于同系物的是,属于同分异构体的是(填入编号)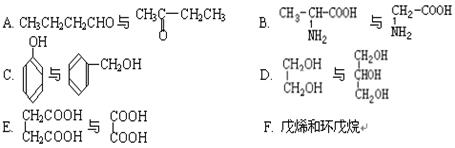
化合物A[KxFe(C2O4)y·zH2O,其中铁元素为+3价]是一种重要的光化学试剂。
(1)制备化合物A的实验流程如下: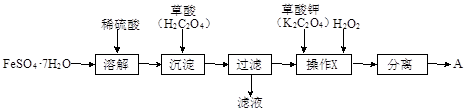
①上述流程中,检验“过滤”后的固体已洗涤干净的方法是。
②上述流程“操作X”中加入H2O2的目的是。
(2)测定化合物A的化学式实验步骤如下:
a、准确称取A样品4.91g,干燥脱水至恒重,残留物质的质量为4.37g;
b、将步骤a所得固体溶于水,加入还原铁粉0.28g,恰好完全反应;
c、另取A样品4.91g置于锥形瓶中,加入足量的3 mol/L的H2SO4溶液和适量蒸馏水,再加入0.50mol/L的KMnO4溶液24.0 mL,微热,恰好完全反应:2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
请通过计算填空:
①4.91g A样品中含结晶水的物质的量为mol。
②A样品中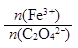 =。③A的化学式为。
=。③A的化学式为。
在下图所示的物质转化关系中,A是用于制造汽车发动机的耐高温陶瓷材料,A由两种元素组成,且两种元素化合价的绝对值相等。常温下,C、F、K是无色无味的气体单质,D、H是固体单质。E是常见的两性氧化物。B、G是汽车尾气中的主要污染气体,所含元素均为第二周期元素。反应②常用于汽车尾气的处理。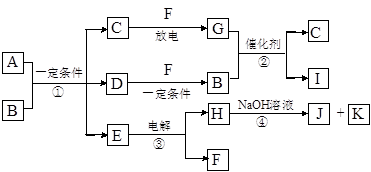
(1)C的电子式。
(2)A的化学式。
(3)反应③的化学方程式。
(4)反应④的离子方程式。