某同学为研究电化学原理,使用KC1盐桥设计如图所示实验装置。下列分析不合理的是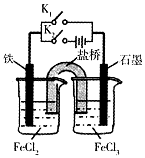
| A.闭合K2断开K1,左侧烧杯中的Fe2+向铁电极移动 |
| B.无论闭合K1断开K2,还是断开K1闭合K2,石墨电极上发生的反应都是Fe3++e-= Fe2+ |
| C.闭合K1断开K2,电流从石墨电极经过K1流向铁电极 |
| D.闭合K1断开K2,左侧烧杯中的溶液pH将逐渐降低 |
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3  K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是()
K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是()
| A.生成40.0LN2(标准状况) | B.有0.250molKNO3被氧化 |
| C.转移电子的物质的量为1.25mol | D.被氧化的N原子的物质的量为3.5mol |
下列离子方程式书写正确的是()。
| A.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
B.将少量SO2通入苯酚钠溶液中:2C6H5O-+SO2+H2O=2C6H5OH+ |
| C.用硫氰化钾溶液可以检验溶液中的Fe3+:Fe3++3SCN-=Fe(SCN)3↓ |
| D.向碘化亚铁溶液中通入过量的氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
短周期元素X、Y、Z、W的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y 的次外层电子数是最外层的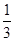 ,ZX2是一种储氢材料,W与Y属于同一主族,下列叙述正确的是()。
,ZX2是一种储氢材料,W与Y属于同一主族,下列叙述正确的是()。
| A.原子半径:rW>rZ>rY |
| B.Y形成的离子与W形成的离子的电子数不可能相同 |
| C.化合物X2Y、ZY、WY3中化学键的类型相同 |
| D.由X、Y、Z、W组成的化合物的水溶液可能显酸性 |
下列说法或表述正确的是( )
①过氧化钠中阳离子和阴离子个数比为1:1
②纯碱既属于正盐又属于钠盐和碳酸盐。
③相同温度下,氢氧化钠溶液的导电能力比氨水溶液强
④丁达尔效应可用于区别溶液和胶体,烟、云、雾均为胶体,能产生丁达尔效应。
⑤钢铁的吸氧腐蚀,负极发生反应:Fe-2e-=Fe2+
| A.①②④⑤ | B.②③④ | C.②④⑤ | D.③④⑤ |
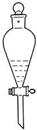
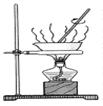
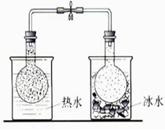
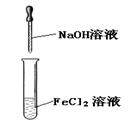
下列实验能达到目的的是()
 |
 |
 |
 |
| 用酒精萃取溴水中的溴 |
将硫酸铜溶液直接蒸干得到胆矾 |
说明2NO2(g)  N2O4(g)△H<0 N2O4(g)△H<0 |
实验室制备Fe(OH)2 |
| A |
B |
C |
D |