Mn(OH)2常用作油漆催干剂。向MnSO4溶液加入NaOH溶液,待沉淀完全后,过滤,洗涤,烘干即可制得Mn(OH)2。
(1)已知:常温下Mn(OH)2的Ksp=1.0×10-15。如果要使溶液中Mn2+沉淀完全,则应该保持溶液中c(OH—)≥ mol·L—1[当c(Mn2+)≤10-5mol/L时,即可认为溶液中Mn2+沉淀完全]。
(2)Mn(OH)2还可以通过MnO2与二氧化硫气体充分接触,再与石灰乳反应制得,写出该反应的总的化学方程式 。
(3)一种含Mn2+的结晶水合物组成为AxMnyBz·mH2O(A表示一种阳离子,B表示一种阴离子)。现称取39.10 g晶体配成100 mL溶液X,取20 mL溶液X,向其中加入足量的氢氧化钠溶液,加热,得到896 mL气体(标准状况);另取20 mL溶液X,向其中加入盐酸,无沉淀产生,再加入BaCl2溶液,产生白色沉淀,过滤,洗涤,烘干,得到固体9.32 g。
①A、B的离子符号分别为 、 。
②通过计算确定该结晶水合物的化学式(写出计算过程)。
写出铜与稀硝酸反应的化学方程式,用单线桥标出电子转移情况
该反应的氧化剂,还原剂,氧化剂和还原剂物质的量之比为。
阿明洛芬属于苯丙酸类抗炎药,镇痛效果优于布洛芬。下图是阿明洛芬的一条合成路线。
⑴反应①为取代反应,该步反应物Me2SO4中的“Me”表示。
⑵E中的官能团有:(写名称)。
⑶写出反应类型:④。
⑷写出F的结构简式。
⑸反应③可以看成是两步反应的总反应,第一步是氰基(—CN)的完全水解反应生成羧基(—COOH), 请写出第二步反应的化学方程式。
⑹化合物 是合成某些药物的中间体。试设计合理方案由化合物
是合成某些药物的中间体。试设计合理方案由化合物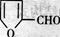 合成
合成 。
。
①合成过程中无机试剂任选;
②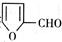 在400摄氏度金属氧化物条件下能发生脱羰基反应;
在400摄氏度金属氧化物条件下能发生脱羰基反应;
③CH2=CH-CH=CH2与溴水的加成以1,4-加成为主;
④合成反应流程图表示方法示例如下:
2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED)。目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、lnGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如下图。试回答:
⑴镓的基态原子的电子排布式是。
⑵砷化镓晶胞中所包含的砷原子(白色球)个数为,与同一个镓原子相连的砷原子构成的空间构型为。
⑶N、P、As处于同一主族,其氢化物沸点由高到低的顺序是。 (用氢化物分子式表示)
⑷砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为。
⑸比较二者的第一电离能:As______Ga(填“<”、“>”或“=”)。
⑹下列说法正确的是(填字母)。
A.砷化镓晶胞结构与NaCl相同 B.GaP与GaAs互为等电子体
C.电负性:As>GaD.砷化镓晶体中含有配位键
现代炼锌的方法可分为火法和湿法两大类,镉是生产硫酸锌的副产品,属于高毒性金属,试回答下列相关问题.
⑴火法炼锌是将闪锌矿(主要含ZnS)通过浮选、焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热至1373-1573K,使锌蒸馏出来。主要反应为:
2ZnS +3O2 2ZnO+2SO2; 鼓风炉中:2C +O2
2ZnO+2SO2; 鼓风炉中:2C +O2 2CO ZnO+CO
2CO ZnO+CO Zn + CO2
Zn + CO2
从火法炼锌蒸馏后的残渣中含多种金属单质及In2O3,可用硫酸提取铟,某研究机构对此研究数据如下。实验中涉及的酸度(每升溶液中含硫酸的质量)与铟的浸出率如下图1;硫酸溶液的体积与固体的体积比如图2
①当酸度为196时,其物质的量浓度为 。
②从节约原料和浸出率考虑,适宜的酸度和液固比分别为:_______、_______。
⑵湿法炼锌的主要工艺流程为:
①从保护环境和充分利用原料角度,如何处理或利用烟气。
②除去酸浸出液中的铁,可用H2O2氧化,再调节pH使之形成Fe(OH)3沉淀,写出H2O2氧化Fe2+的离子方程式。
③酸浸出液还含有Cd2+,为了防止镉污染并回收镉,根据它们性质的差异,可用氢氧化钠溶液分离,已知Zn(OH)2和氢氧化铝一样也具有两性,试写出分离的离子方程式____________________、_______________。
甲醇是一种很好的燃料,工业上用CH4和H2O为原料,通过反应Ⅰ和Ⅱ来制备甲醇。
⑴将1.0 mol CH4和2.0 mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应:
CH4(g)+H2O(g) CO(g)+3H2(g)……Ⅰ。CH4的转化率与温度、压强的关系如上图。
CO(g)+3H2(g)……Ⅰ。CH4的转化率与温度、压强的关系如上图。
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为。
②图中的P1P2(填“<”、“>”或“=”),100℃时平衡常数为。
③该反应的△H0(填“<”、“>”或“=”)。
⑵在压强为0.1 MPa条件下,将a mol CO与 3amol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g) CH3OH(g);△H<0……Ⅱ。
CH3OH(g);△H<0……Ⅱ。
④若容器容积不变,下列措施可增加甲醇产率的是。
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
⑤为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。

A.则上表中剩余的实验条件数据:a=________、b=_______。
B.根据反应Ⅱ的特点,右上图是在压强分别为0.1MPa和5MPa下CO的转化率随温度变化的曲线图,请指明图中的压强Px=_________MPa。