[实验化学]
水杨酸可用于制备解热镇痛药阿司匹林。重结晶纯化固体水杨酸的步骤如下:
步骤1:按图1所示装置,在圆底烧瓶中加入1.2 g粗水杨酸,10 mL 30%乙醇和磁子。接通冷凝水后,搅拌加热至沸,直到完全溶解。
步骤2:冷却后,加入活性炭,重新搅拌加热煮沸几分钟后,利用图2装置趁热过滤到锥形瓶中,并在短颈漏斗上盖好表面皿。
步骤3:盛滤液的锥形瓶用塞子塞好,自然冷却后再用冰水冷却,析出水杨酸晶体。
步骤4:用图3所示装置进行抽滤,用少量30%的乙醇洗涤。抽干后得到的晶体转移到表面皿上,放入干燥器中干燥。
步骤5:称量干燥后固体质量为0.81 g。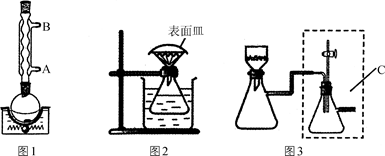
(1)步骤1中接通冷凝水时,冷水应从________(填“A”或“B”)端进。
(2)步骤2中“趁热过滤”的目的是______________________。
(3)步骤3中“自然冷却后再用冰水冷却”,而不直接用冰水浴冷却的目的是________。
(4)步骤4中C装置的作用是______________________________________。
(5)本次实验中,水杨酸的收率为________。确定最终产品是水杨酸的实验或方法是___________。
某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考察其化学性质,首先做了银镜反应。
(1)在甲酸进行银镜反应前,必须在其中加入一定量的,因为。
(2)写出甲酸进行银镜反应的化学方程式。
(3)某同学很成功的做了银镜反应,他肯定没有进行的操作(写字母)
| A.用洁净试管 |
| B.在浓度为2%的NH3·H2O中滴入稍过量的浓度为2%的硝酸银 |
| C.用前几天配制好的银氨溶液 |
| D.在银氨溶液里加入稍过量的甲酸 |
E.用小火对试管直接加热
F.反应过程中,振荡试管使之充分反应
然后,同学们对甲酸与甲醇进行了酯化反应的研究: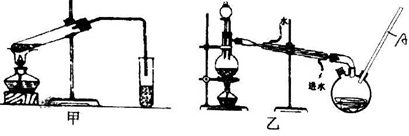
(4)乙装置中长导管A的作用是。
(5)写出甲酸和甲醇进行酯化反应的化学方程式。
(6)选择甲装置还是乙装置好?,原因是。
(7)实验过程中选用的药品及试剂有:浓H2SO4、甲醇、甲酸还有、两种必备用品。
(8)一同学用装有饱和氢氧化钠的三颈瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释。
为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置: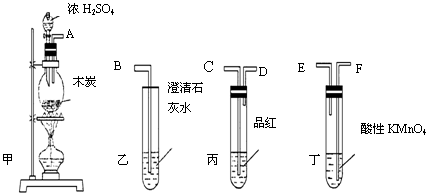
(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):
接,接,接;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?
乙中,丙中;
(3)丁中酸性KMnO4溶液的作用是;
(4)写出甲中反应的化学方程式。
根据我国目前汽车业发展速度,预计2020年汽车保有量超过2亿辆,中国已成为全球最大的汽车市场。因此,如何有效处理汽车排放的尾气,是需要进行研究的一项重要课题。目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO 2CO2+N2。为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究。
2CO2+N2。为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究。
【资料查阅】①不同的催化剂对同一反应的催化效率不同;
②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响。
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
(1)完成以下实验设计表(表中不要留空格)。
| 实验 编号 |
实验目的 |
T/℃ |
NO初始浓度 mol/L |
CO初始浓度 mol/L |
同种催化剂 的比表面积m2/g |
| Ⅰ |
为以下实验作参照 |
280 |
6.50×10-3 |
4. 00×10-3 |
80 |
| Ⅱ |
① |
② |
③ |
④ |
120 |
| Ⅲ |
探究温度对尾气转化速率的影响 |
360 |
⑤ |
⑥ |
80 |
【图像分析与结论】利用气体传感器测定了三组实验中CO浓度随时间变化的曲线图,如下:
(2)计算第Ⅰ组实验中,达平衡时NO的浓度为__________________;
(3)由曲线Ⅰ、Ⅱ可知,增大催化剂比表面积,汽车尾气转化速率_____________(填“增大”、“减小”、“无影响”);
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。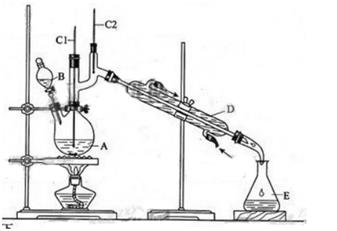
发生的反应如下:CH3CH2CH2CH2OH CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| 沸点/℃ |
密度/(g·cm-3) |
水中溶解性 |
|
| 正丁醇 |
11.72 |
0.8109 |
微溶 |
| 正丁醛 |
75.7 |
0.8017 |
微溶 |
实验步骤如下:
将6.0 g Na2Cr2O7放入100 mL烧杯中,加30 mL水溶解,再缓慢加入5 mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0 g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90—95 ℃,在E中收集90 ℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75—77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,(填“能”或“不能”)将Na2Cr2O7溶液加到浓硫酸中,说明理由。
(2)加入沸石的作用是。若加热后发现未加沸石,应采取的正确方法是。
(3)上述装置图中,B仪器的名称是,D仪器的名称是。
(4)分液漏斗使用前必须进行的操作是(填正确答案标号)。
a.润湿b.干燥c.检漏d.标定
(5)将正丁醛粗产品置于分液漏斗中分液时,水在层(填“上”或“下”)
(6)反应温度应保持在90—95 ℃,其原因是。
(7)本实验中,正丁醛的产率为%。
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生成过程。
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若,则整个装置气密性良好。装置D的作用是。装置E中为溶液。
(2)装置A中反应的化学方程式为。
烧瓶C中发生反应如下:
Na2S+H2O+SO2=Na2SO3+H2S(I)
2H2S+SO2=3S+2H2O(II)
S+Na2SO3 Na2S2O3(III)
Na2S2O3(III)
为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为。