下图曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,下列叙述正确的是( )
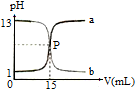
| A.NaOH溶液的浓度为0.1 mol·L-1 |
| B.P点时恰好完全反应,溶液呈中性 |
| C.曲线a是盐酸滴定氢氧化钠溶液的测定曲线 |
| D.本实验的指示剂不能用甲基橙,只能用酚酞 |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是
| A.2.24LCl2中含有的原子数一定为0.2 ×6.02×1023 |
| B.0.1L2mol·L-1的Na2CO3溶液中含有的CO32-数目为0.2 ×6.02×1023 |
| C.0.88gC3H8中含有的共价键总数目为0.2 ×6.02×1023 |
| D.7.8g过氧化钠粉末与水反应转移的电子数为0.2 ×6.02×1023 |
下列说法不正确的是
A.BaCrO4(s)  Ba2+(aq)+ CrO42-(aq)的平衡体系中,加入BaCl2浓溶液沉淀量增多 Ba2+(aq)+ CrO42-(aq)的平衡体系中,加入BaCl2浓溶液沉淀量增多 |
| B.pH=2的酸溶液与pH=12的强碱溶液等体积混合,所得溶液pH≤7 |
C.苯酚显色原理为:6C6H5OH+Fe3+ Fe(C6H5O)63-(紫色)+6H+,则检验水杨酸( Fe(C6H5O)63-(紫色)+6H+,则检验水杨酸( )中的酚羟基,需加入适量的小苏打溶液后,再加入氯化铁溶液 )中的酚羟基,需加入适量的小苏打溶液后,再加入氯化铁溶液 |
| D.某试液中加入盐酸酸化的氯化钡溶液有白色淀淀,该试液中一定含有SO42- |
X、Y、Z是三种短周期元素,在周期表中的相对位置如图所示,有关说法正确的是
| A.X、Y、Z可以都是金属 X Y Z |
| B.原子半径Z>Y>X |
| C.最高价氧化物对应的水化物酸性Z>Y>X |
D.X、Y、Z可形成 分子,若Z、X原子满足8电子结构, 分子,若Z、X原子满足8电子结构, |
则Y原子也满足8电子结构
LiAlH4( )、LiH是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是
)、LiH是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是
| A.LiH与D2O反应,所得氢气的摩尔质量为4g/mol |
| B.1molLiAlH4在125℃完全分解,转移3mol电子 |
| C.LiAlH4溶于适量水得到无色溶液,则化学方程式可表示为:LiAlH4+2H2O=LiAlO2+4H2↑ |
| D.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂 |
下列实验操作正确的是
| A.用蒸发溶剂的方法,将氯化铁稀溶液蒸发浓缩为饱和溶液 |
| B.氢氟酸储存在带玻璃塞的棕色试剂瓶中 |
| C.金属钾储存在煤油中 |
| D.实验室制取乙烯时,常含有少量的CO2、SO2及H2O(g)杂质,可依次通过高锰酸钾溶液和碱石灰得较纯净的乙烯气体 |