研究物质的合成或制备是有机化学、无机化学的重要任务之一。
(1)某实验小组探究实验室制备无水氯化镁的方法,设计了以下装置: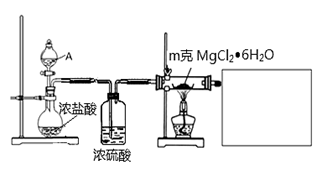
①分液漏斗中的A物质是________________(填试剂名称)。
②利用中学常见的仪器,在答题卡中补充完整实验装置(不必画出夹持装置)。可选择的试剂有:稀NaOH溶液、无水氯化钙、稀硫酸、浓硫酸。
③假设实验过程中MgCl2▪6H2O未水解,不用任何试剂用最简单的方法检验MgCl2▪6H2O是否完全转化为MgCl2。写出实验方法________________。
④工业生产中得到无水氯化镁可用于电解制备镁单质,电解装置中,镁在____极析出。
(2)实验室制备并收集纯净乙烯
①有的同学通过乙醇发生消去反应进行实验。除乙醇外,所需的试剂或用品(不包括仪器)有_________________。
②有的同学探究其它制备乙烯的方法,他设计了以下装置制备乙烯。实验结果是量筒内壁附着较多无色油状液体,且得到很少量的气体,请分析气体产率很低的原因主要是______________________。为增大气体产率,在下图装置的基础上,提出一点改进措施__________________。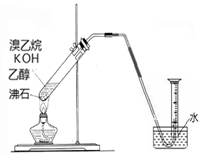
从实验安全角度考虑,该实验很可能发生的问题是________________。
已知理想气体各参数p(压强)、V(体积)、T(温度)、n(物质的量)满足理想气体状态方程pV=nRT。某学校课外活动小组粗略测定理想气体状态方程中气体常数R的值,下面是测定实验的分析报告,请填写有关空白: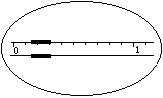
(一)测定原理:在理想气体状态方程pV=nRT中,气体常数R=pV/nT的数值可以通过实验来确定。本实验通过金属镁置换出盐酸中的氢来测定R的值。其反应为:
Mg+2HCl=MgCl2+H2↑
如果称取一定质量的镁与过量的盐酸反应,则在一定温度和压力下,可以通过测出反应放出氢气的体积。实验室的温度和压力可以分别由温度计和气压计测得。氢气物质的量可以通过反应中镁的质量来求得。将以上所得各项数据代入R=" pV" /nT式中,即可算出R值。
(二)实验用品及试剂:①仪器:托盘天平、测定气体常数的装置(如上图所示);②试剂:6mol·L-1HCl、镁条若干。
(三)实验内容:
1.在托盘天平上称出镁条的质量(称量镁条天平的游码示数如右图所示,未用砝码,单位为g);
2.按上图搭好仪器。取下试管,移动量气管B,使量气管A中的水面略低于零刻度线,然后将量气管B固定。
3.在试管中加入15mL 6 mol·L-1HCl,不要使盐酸沾湿试管的上半部。将已称重的镁沾少许水,贴在试管上部不与盐酸接触。
4.检查仪器是否漏气,方法如下:(方法要求简单有效)
。
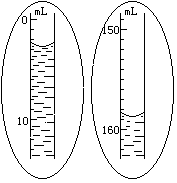
5.如果装置不漏气,调整量气管B的位置,使量气管A内水面与量气管B 内水面在同一水平面上(要求“在同一水平面上”的原因是;实现“在同一水平面上”的操作是),然后准确读出量气管A内水面凹面最低点的读数V1(如右图所示)。
6.轻轻摇动试管,使镁条落入盐酸中,镁条与盐酸反应放出氢气。此时量气管A内水面即开始下降。为了不使量气管A内气压增大而造成漏气,在量气管A内水面下降的同时,慢慢(上或下)移量气管B,使两管内的水面基本保持水平。反应停止后,待试管冷却至室温(约10分钟),移动量气管B,使两管内的水面相平,读出反应后量气管A内的精确读数V2(如右图所示)。
7.记录实验时的室温t和大气压P。(已知室温为27℃,大气压为100kPa)
(四)数据记录与处理(在横线上填写适当内容):
| 镁条的质量 |
w= |
g |
|
| 氢气的物质的量 |
n= |
mol |
|
| 反应前量气管A内读数 |
V1= |
ml |
|
| 反应后量气管A内读数 |
V2= |
ml |
|
| 氢气的体积 |
V |
ml |
|
| 室温 |
T |
K |
|
| 大气压 |
P |
Pa |
气体常数R的值(计算过程和结果):
(五)问题与讨论:①在读取量气管内气体体积V1时,眼睛仰视读数,结果造成R的测定值(偏高、偏低或无影响);②若没等反应试管冷却到室温就量取液面的高度,结果造成R的测定值(偏高、偏低或无影响)。
用下列仪器、药品验证由铜和适量浓硝酸反应产生的气体中含NO(仪器从图示所列中选用,N2和O2的用量可自由控制)。已知:①NO+NO2+2OH-→2NO+H2O②气体液化温度:NO2 21℃,NO-152℃
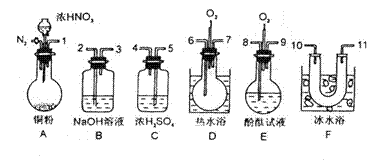 |
试回答:
(1)仪器的连接顺序(按左→右连接,填各接口的编号)为。
(2)反应前应通入N2,目的是。
(3)装置F的作用是。
(4)确认气体中含NO的现象是。
(5)若通入O2过量则B中反应的化学方程式为。
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物,该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉,这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”,请分别用下图中示意的两套仪器装置,制取上速铁的氧化物和“引火铁”,实验中必须使用普通铁粉、6molL-1盐酸,其它试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。
填写下列空白:
(1)实验进行时试管A中应加入的试剂是
烧瓶B的作用是;
烧瓶C的作用是
在试管D中收集得到的是
(2)实验时,U型管G中应加入的试剂是
分液漏斗H中应加入
(3)两套装置中,在实验时需要加热的仪器是(填该仪器对应字母)
(4)烧瓶I中发生的反应有时要加入少量硫酸铜溶液,其目的是
(5)试管E中发生反应的化学方程式是
(6)为了安全,在E管中的反应发生前,在F出口处必须;E管中反应开始后,在F出口处应
“卤块”的主要成分为MgCl2(含Fe2+、Fe3+、Mn2+等杂质离子),若以它为原料,按如下工艺流程图,即可制得“轻质氧化镁”。如果要求产品尽量不含杂质离子,而且成本较低,流程中所用试剂或PH值控制可参考下列附表确定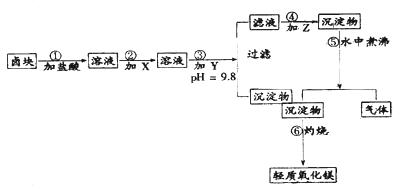
轻质氧化镁生产工艺流程图
表1生成氢氧化物沉淀的PH值
| 物质 |
开始沉淀 |
沉淀完全 |
| Fe(OH)3 Fe(OH)2 Mn(OH)2 Mg(OH)2 |
2.7 7.6 8.3 9.6 |
3.7 9.6 9.8 11.1 |
*)注:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常常将它氧化成为Fe3+,生成
Fe(OH)3沉淀而去除之。
表2化学试剂价值表
| 试剂 |
价格(元/t) |
| 漂液(含NaClO25.2%) H2O2(30%) NaOH(固98%) Na2CO3(固99.5%) 卤块(MgCl2,30%) |
450 2400 2100 600 310 |
请填写以下空白:
(1)在步骤②加入的试剂X,最佳选择应是,其作用是。
(2)步骤③加入的试剂Y应是;之所以要控制pH=9.8,其目的是。
(3)在步骤⑤时发生的化学反应方程式是:
请你选用下图所示仪器和药品,按实验室要求,设计一套完整的检验一氧化碳还原性和二氧化碳化学性质的实验,并回答下列问题:
实验药品:盐酸、石灰石、氧化铜粉末、木炭粉、氢氧化钙溶液。
(1)实验装置连接顺序依次为(用字母表示)___________;
(2)A装置的药品是_________,发生反应的化学方程式为_______________________;
(3)B装置中产生的实验现象是_________,发生反应的化学方程式为____________
(4)C装置中发生反应的化学方程式为____________________________________;
(5)D装置中产生的现象是_________;
(6)尾气中含有毒气体,排放到空气中会造成污染,处理方法是_________。