天然油脂结构的核心为甘油[HOCH2CH(OH)CH2OH],有一瘦身用的非天然油脂,其结构的核心则为蔗糖(C12H22O11)。该非天然油脂可由直链型的不饱和油酸(C17H33COOH)与蔗糖反应而得,其反应示意图如下图所示(注意图中的反应式不完整)。
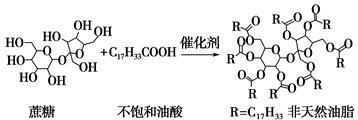
下列说法正确的是( )
| A.蔗糖酯属于油脂类物质 |
| B.该非天然油脂为高分子化合物 |
| C.该非天然油脂与氢氧化钠溶液共热,其水解产物不与溴水反应 |
| D.该蔗糖酯在稀硫酸的作用下水解,最终可生成三种有机化合物 |
一定温度下,在一个容积为1 L的密闭容器中,充入1 mol H2(g)和1 mol I2(g),发生反应H2(g)+I2(g) 2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,在该温度下,在另一个容积为2 L的密闭容器中充入1 molHI(g)发生反应HI(g)
2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,在该温度下,在另一个容积为2 L的密闭容器中充入1 molHI(g)发生反应HI(g) 1/2 H2(g)+ 1/2 I2(g),则下列判断正确的是
1/2 H2(g)+ 1/2 I2(g),则下列判断正确的是
| A.后一反应的平衡常数为1 |
| B.后一反应的平衡常数为0.5 |
| C.后一反应达到平衡时,H2的平衡浓度为0.25 mol·L-1 |
| D.后一反应达到平衡时,HI(g)的平衡浓度为0.5 mol·L-1 |
反应N2O4(g) 2NO2(g)ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g)ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是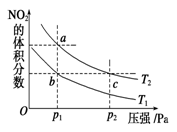
| A.a、c两点的反应速率:a>c |
| B.a、c两点气体的颜色:a深、c浅 |
| C.a、b两点气体的平均相对分子质量:a>b |
| D.b、c两点化学平衡常数:b<c |
在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2 SO2(g)+O2(g) 2SO3(g)△H<0 。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量Q kJ,则下列分析正确的是
2SO3(g)△H<0 。2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量Q kJ,则下列分析正确的是
| A.在该条件下,反应前后的压强之比为6 : 5.3 |
| B.若反应开始时容器体积为2L,则v(SO3)=0.35mol/(L·min) |
| C.若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4mol |
| D.若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量大于Q kJ |
已知100℃时,水的离子积常数KW=1×10-12,对于该温度下pH为1的硫酸,下列叙述正确的是
| A.向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和 |
| B.该溶液中硫酸电离出的c(H+)与水电离出的c(H+)之比为10-10 |
| C.等体积的该硫酸与室温下pH为1的硫酸中和碱的能力相同 |
| D.该溶液中水电离出的c(H+)是pH为3的硫酸中水电离出的c(H+)的100倍 |
一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2 CH3OH (g) CH3OCH3(g)+H2O(g),则下列说法正确的是
CH3OCH3(g)+H2O(g),则下列说法正确的是
| 容器 编号 |
温度(℃) |
起始物质的量(mol) |
平衡物质的量(mol) |
|
| CH3OH (g) |
CH3OCH3(g) |
H2O (g) |
||
| I |
387 |
0.20 |
0.080 |
0.080 |
| Ⅱ |
387 |
0.40 |
||
| Ⅲ |
207 |
0.20 |
0.090 |
0.090 |
A.该反应的正方向应为吸热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行