北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。已知:
①C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)ΔH1=+156.6 kJ·mol-1
②CH3CH===CH2(g)→CH4(g)+HC≡CH(g)ΔH2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g)→CH3CH===CH2(g)+H2(g)的ΔH=________kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为________________;放电时,CO32-移向电池的________(填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3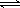 HCO3-+H+的平衡常数K1=________(已知:10-5.60=2.5×10-6)。
HCO3-+H+的平衡常数K1=________(已知:10-5.60=2.5×10-6)。
配平下列氧化还原反应方程式
Cu2++FeS2+ ====Cu2S+
====Cu2S+ +Fe2++
+Fe2++
配平□P4O+□Cl2——□POCl3+□P2Cl5。
配平方程式:
□SO2+□H2S——□S+□H2S
一个体重50 kg的健康人含铁2 g。这2 g铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。二价铁离子(亚铁离子)易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁(FeSO4)。服用维生素C,可以使食物中的铁离子(三价铁离子)变成亚铁离子,有利于铁的吸收。
(1)人体中经常进行Fe2+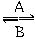 Fe3+的转化,A中Fe2+作_________剂,B中Fe3+作_______剂。
Fe3+的转化,A中Fe2+作_________剂,B中Fe3+作_______剂。
(2)从“服用维生素C,可以使食物中的铁离子变成亚铁离子”这句话分析出维生素C在这一反应中作______________剂,具有_________________性。
已知下列3个反应:
16HCl(浓)+2KMnO4====2KCl+2MnCl2+8H2O+5Cl2↑ ①
4HCl(浓)+MnO2 MnCl2+2H2O+Cl2↑ ②
MnCl2+2H2O+Cl2↑ ②
4HCl(浓)+O2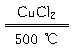 2H2O+2Cl2↑ ③
2H2O+2Cl2↑ ③
试完成下列问题:
(1)3个反应中的还原剂___________________(选填字母)。
| A.都是浓盐酸 | B.都是HCl |
| C.只有2个反应是HCl | D.只有1个反应是HCl(aq) |
(2)KMnO4、MnO2、O2的氧化性强弱顺序为_______________________。