天然气、氨在工农业生产中具有重要意义。
(1)25 ℃、l0l kPa时,32 g CH4完全燃烧生成稳定的氧化物时放出1780.6 kJ的热量,写出该反应的热化学方程式________________________________。
(2)合成氨用的氢气,工业上可利用“甲烷蒸气转化法生产氢气”,反应为:CH4(g)+H2O(g) CO(g)+3H2(g),已知有关反应的能量变化如下图:
CO(g)+3H2(g),已知有关反应的能量变化如下图: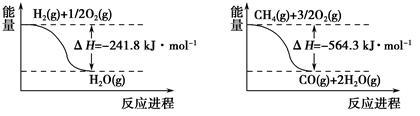
则该反应的焓变ΔH=______________________________________。
(15分)铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得.
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如图1所示:
图1
图2
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如图2所示:
回答下列问题:
(1)写出反应1的化学方程式 ; 。
(2)滤液Ⅰ中加入CaO生成的沉淀是______,反应2的离子方程式为______;
(3)E可作为建筑材料,化合物C是______,写出由D制备冰晶石的化学方程式______;
(4)电解制铝的化学方程式是______,以石墨为电极,阳极产生的混合气体的成分是______。
将海水淡化和与浓海水资源化结合起来是综合利用海水的重要途径之一。一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产品。回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是 (填序号)。
①用混凝法获取淡水②提高部分产品的质量
③优化提取产品的品种④改进钾,溴,镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收。碱吸收溴的主要反应是:Br2+Na2CO3+H2O NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为 mol。
NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为 mol。
(3)海水提镁的一段工艺流程如下图: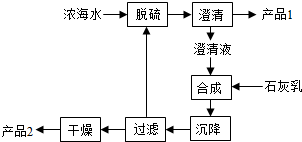
浓海水的主要成分如下:
| 离子 |
Na+ |
Mg2+ |
Cl- |
SO42- |
| 浓度/(g·L-1) |
63.7 |
28.8 |
144.6 |
46.4 |
该工艺过程中,脱硫阶段主要反应的离子方程式为 ,产品2的化学式为 ,1L浓海水最多可得到产品2的质量为 g。
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为 ;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式 。
二氧化硫、一氧化碳、氮的氧化物、氨气都是非常重要的非金属化合物,研究这些化合物对环境保护、理解化学反应原理都具有重要意义。
(1)二氧化氮与一定量空气混合通入水中能被水完全吸收,反应的化学方程式为_________________。若该反应有a×NA个电子转移,则参加反应的二氧化氮的物质的量为________。
(2)下列除去大气污染物的化学方程式不正确的是________。
A.汽车尾气经催化剂作用:CO+NO NO2+C
NO2+C
B.石灰乳吸收硫酸厂尾气:SO2+Ca(OH)2===CaSO3+H2O
C.燃烧法除去尾气中硫化氢:2H2S+3O2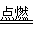 2SO2+2H2O
2SO2+2H2O
D.氨气与一氧化氮在一定条件下反应:4NH3+6NO 5N2+6H2O
5N2+6H2O
(3)大多数非金属氧化物能被氢氧化钠溶液吸收。例如,NaOH+SO2=NaHSO3,2NaOH+SO2=Na2SO3+H2O,2NO2+2NaOH=NaNO3+NaNO2+H2O,NO+NO2+2NaOH=2NaNO2+H2O,NO不溶于氢氧化钠溶液或水。
①同种反应物,其反应产物与浓度、温度、反应物相对量等因素有关。影响二氧化硫与氢氧化钠反应产物的因素与下列反应相同的是________。
A.木炭与氧气反应
B.硫与氧气反应
C.钠与氧气
D.铜与硝酸溶液反应
②某NO与NO2混合气体通入氢氧化钠溶液被完全吸收,推测混合气体中气体组成为________。
A. =1 B.
=1 B. ≤1 C.
≤1 C. ≥1 D.无法判断
≥1 D.无法判断
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采取下面的工艺流程生产单质碘。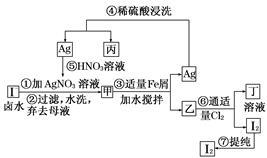
试回答下列问题:
(1)乙、丁中溶质的化学式:乙:________,丁________。
(2)第④步操作中用稀硫酸浸洗的目的是________(填写字母编号)。
| A.除去未反应的NO | B.除去未反应的I- |
| C.除去未反应的Fe | D.除去碱性物质 |
(3)第⑦步操作可供提纯I2的两种方法是________和________(不要求写具体步骤)。
(4)实验室检验I2的方法是___________________________________________________。
(5)甲物质见光易变黑,其原因是(用化学方程式表示)__________________。
过渡金属元素及其化合物的应用广泛,是科学家们进行前沿研究的方向之一。
(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉做显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰。相关的反应如下:
4FeCl3+2NH2OH•HCl=4FeCl2+N2O↑+6HCl+H2O
①基态Fe原子中,电子占有的最高能层符号为__________,核外未成对电子数为__________,Fe3+在基态时,外围电子排布图为______________________________。
②羟胺中(NH2OH)采用sp3杂化的原子有_______________,三种元素电负性由大到小的顺序为________;与ClO4-互为等电子体的分子的化学式为_______________________。
(2) 过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合18电子规则。如Cr可以与CO形成Cr(CO)6分子:价电子总数(18)=Cr的价电子数(6)+CO提供电子数(2×6)。Fe、Ni两种原子都能与CO形成配合物,其化学式分别为_____________、______________。
(3) Pt2+的常见配合物Pt(NH3)2Cl2存在两种不同的结构:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度较小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。
①Q是_________________分子(选填“极性”或“非极性”)。
②P分子的结构简式为__________________________。
(4)NiXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,晶胞边长为a pm。晶胞中两个Ni原子之间的最短距离为___________pm。若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2﹢与Ni3﹢的最简整数比为_________。