已知在等温等压条件下,化学反应方向的判据为:ΔH-T△S < 0反应自发进行(其中ΔH为焓变,△S为熵变,T为热力学温标,单位为K)。设反应A(s)=D(g)+E(g) 的ΔH-T∆S=(-4500+11T)J/mol ,要防止反应发生,温度必须
| A.高于409K | B.低于136K |
| C.高于136K而低于409K | D.409K |
已知25℃、101 kPa下,金刚石、石墨燃烧的热化学方程式分别为:
C(石墨,s)+O2(g)="==" CO2(g)△H=-393.51 kJ• mol-1
C(金刚石,s)+O2(g)="==" CO2(g)△H=-395.41 kJ• moL-1
据此判断,下列说法正确的是
| A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低 |
| B.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低 |
| C.由石墨制备金刚石是吸热反应;金刚石比石墨稳定 |
| D.由石墨制备金刚石是放热反应;石墨比金刚石稳定 |
化学反应N2+3H2 2NH3的能量变化如下图所示,该反应的热化学方程式是
2NH3的能量变化如下图所示,该反应的热化学方程式是
A.N2(g)+3H2(g) 2NH3(1) △H=2(a-b-c)kJ·mol-1 2NH3(1) △H=2(a-b-c)kJ·mol-1 |
B.N2(g)+3H2(g) 2NH3(g) △H=2(b-a)kJ·mol-1 2NH3(g) △H=2(b-a)kJ·mol-1 |
C.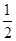 N2(g)+ N2(g)+ H2(g) H2(g)  NH3(1) △H=(b+c-a)kJ·mol-1 NH3(1) △H=(b+c-a)kJ·mol-1 |
D.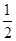 N2(g)+ N2(g)+ H2(g) H2(g) NH3(g) △H=(a+b)kJ·mol-1 NH3(g) △H=(a+b)kJ·mol-1 |
一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应:2SO2+O2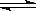 2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是
2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是
| A.2 mol SO2+ 1 mol O2 |
| B.4 mol SO2+ 1 mol O2 |
| C.2 mol SO2+ 1 mol O2+ 2mol SO3 |
| D.3 mol SO2+0.5mol O2+ 1molSO3 |
0.1mol·L -1NaHCO3溶液的pH最接近于
| A.5.6 | B.7.0 | C.8.4 | D.13.0 |
把500mL有BaCl2和KCl的混合溶液分成5等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
| A.0.1(b-2a)mol/L | B.10(2a-b)mol/L |
| C.10(b-a)mol/L | D.10(b-2a)mol/L |