人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(Ca2C2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用酸性KMnO4溶液定量反应即可测定血样样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
【实验探究一】配制酸性KMnO4标准溶液。如上图所示是配制100mL 酸性KMnO4标准溶液的过程示意图。
(1)请你观察图示判断其中不正确的操作有____________(填序号);
(2)其中确定100mL溶液体积的容器是____________(填名称);
(3)如果按照图示的操作所配制溶液进行实验,在其他操作均正确的情况下,所得KMnO4溶液浓度将_________(填“偏大”或“偏小”)。
【实验探究二】测定血液样品中Ca2+的浓度,抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol/L 酸性KMnO4溶液与之反应,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
(4)已知草酸跟KMnO4反应的离子方程式为:2MnO4-+5H2C2O4+6H+═2Mnx++10CO2↑+8H2O则式中的x=_________
(5)经过计算,血液样品中Ca2+的浓度为___________ mg/cm3。
如图在试管甲中先加入2mL 95%的乙醇, 并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验。试回答: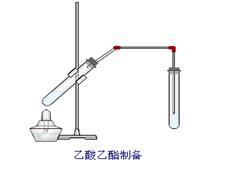
(1)试管甲中加入浓硫酸的目的是
(2)该实验中长导管的作用是 ,其不宜伸入试管乙的溶液中,原因是
(3)试管乙中饱和Na2CO3的作用是
(4)试管乙中观察到的现象是
(5)液体混合加热时液体容积不能超过其容积的,本实验反应开始时用小火加热的原因是;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
(6)写出试管甲中发生反应的化学方程式。
某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大___________,原因是___________________________________________________。
(2)哪一时间段的反应速率最小___________,原因是_____________________。
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变) ___________。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:A.蒸馏水、B.NaCl溶液、C.NaNO3溶液、D.CuSO4溶液、E.Na2CO3溶液,你认为可行的是___________。
(5)把锌与盐酸的反应设计成原电池,请画出装置示意图,标明正负极,电子流动方向,写出正极的电极反应式________________________。
实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的SO2。某同学设计下列实验以确定上述混合气体中含有乙烯和SO2。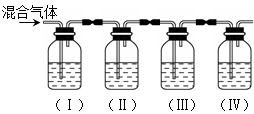
(1)I、II、III、IV装置可盛放的试剂是:I:II:III:IV:(请将下列有关试剂的序号填入空格内)。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.溴水 |
(2)能说明SO2气体存在的现象是;
使用装置II的目的是;
使用装置III的目的是;
确定含有乙烯的现象是。
(3)Ⅳ中发生反应的化学方程式为;产物的名称是。
阿司匹林可由水杨酸与乙酸酐作用制得。其制备原理如下:
主反应: +化合物A
+化合物A
水杨酸乙酸酐阿司匹林(乙酰水杨酸)
副反应:
聚水杨酸
已知:① 水杨酸可溶于水,乙酰水杨酸的钠盐易溶于水,聚水杨酸(固体)难溶于水;
② 阿司匹林,白色针状或板状结晶或粉末,微溶于水;阿司匹林可按如下步骤制取和纯化:
步骤1:在干燥的50 mL圆底烧瓶中加入2 g水杨酸、5 mL乙酸酐和5滴浓硫酸,振荡使水杨酸全部溶解;
步骤2:按图所示装置装配好仪器,通水,在水浴上加热5~10min,用电炉控制温度在85~90℃;
步骤3:反应结束后,取下反应瓶,冷却,再放入冰水中冷却、结晶、过滤、冷水洗涤2~3次,继续过滤得粗产物;
步骤4:将粗产物转移至150 mL烧杯中,在搅拌下加入25 mL饱和碳酸氢钠溶液,充分搅拌,然后过滤;
步骤5:将滤液倒入10 mL 4 mol/L盐酸溶液,搅拌,将烧杯置于冰浴中冷却,使结晶完全。过滤,再用冷水洗涤2~3次。
(1) 主反应中,生成物中化合物A是____________;
(2) 步骤2组装仪器还需要一种玻璃仪器,名称是________,该仪器的位置如何摆放?____________________________;冷凝管的作用是_________,冷凝管通水,水应从______(填“a”或“b”)口进。
(3) 步骤4过滤得到的固体为________;
(4) 经过步骤5得到产物,发生反应的化学方程式为______________________;
(5) 最后得到的阿司匹林可能会有少量未反应的水杨酸。如何用实验的方法检验步骤5中得到的晶体是否含有水杨酸?___________________________________。若阿司匹林晶体含有水杨酸,还需要采用________方法,进一步纯化晶体。
二氧化铈 是一种重要的稀土氧化物.。平板电视显示屏生产过程中产生大量的废玻璃粉末(含
是一种重要的稀土氧化物.。平板电视显示屏生产过程中产生大量的废玻璃粉末(含 以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
(1)洗涤滤渣A的目的是为了去除(填离子符号),检验该离子是否洗净的方法是。
(2)第②步反应的离子方程式是,滤渣B的主要成分是。
(3)萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP(填“能”或“不能”)与水互溶。实验室进行萃取操作是用到的主要玻璃仪器有、烧杯、玻璃棒、量筒等。
(4)取上述流程中得到的
 产品0.536g,加硫酸溶解后,用0.1000mol•
产品0.536g,加硫酸溶解后,用0.1000mol• 溶液(铈被还原为
溶液(铈被还原为 ),消耗25.00mL溶液,该产品中
),消耗25.00mL溶液,该产品中 的质量分数为。
的质量分数为。