某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。

(1)写出装置A发生反应的离子方程式 。
若用含有0.2mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12L的原因是
(2)①装置B中盛放的试剂名称为 ,现象是 。
②装置D和E中出现的不同现象说明的问题是 。
③装置F的作用是 。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 与 之间(填装置字母序号),装置中应放入 (填写试剂或用品名称)。
(8分)下面a~e是中学化学实验中常见的几种定量仪器:
(a)量筒 (b)容量瓶 (c)滴定管 (d)托盘天平 (e)温度计
(1)其中标示出仪器使用温度的是(填写编号)。
(2)能够用以精确量取液体体积的是(填写编号)。
(3)由于错误操作, 使得到的数据比正确数据偏小的是(填写编号)。
| A.用量筒量取一定量液体时, 俯视液面读数。 |
| B.中和滴定达终点时俯视滴定管内液面读数。 |
| C.没有用蒸馏水洗烧杯2—3次,并将洗液移入容量瓶中。 |
| D.容量瓶刚用蒸馏水洗净,没有烘干。 |
E、定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切。
F、把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用。
G.使用容量瓶配制溶液时, 俯视液面定容后所得溶液的浓度。
(4)称取10.5g固体样品(1g以下使用游码)时, 将样品放在了天平的右盘, 则所称样品的实际质量为g。
某同学在实验室欲配制物质的量浓度均为1.0 mol/L的NaOH溶液和稀H2SO4各450mL。提供的试剂是:NaOH固体和98%的浓H2SO4(密度为1.84 g/cm3)及蒸馏水。
(1)配制两种溶液时都需要的玻璃仪器是____________________________________ 。
(2)应用托盘天平称量NaOH ___________g,应用量筒量取浓H2SO4________mL。
(3)配制时,先要检查容量瓶是否漏水,其方法是 。
。
(4)浓硫酸溶于水的正确操作方法是___________ _____。
_____。
(5)在配制上述溶液实验中,下列操作引起结果偏低的有_________________
| A.该学生在量取浓硫酸时,俯视刻度线 |
| B.称量固体NaOH时,将砝码和物品的位置颠倒(没有使用游码) |
C.溶解H2SO4操作时没有冷却至室温就立即完成后面的配制操 作。 作。 |
D.在烧杯中溶解 搅拌时,溅出少量溶液 搅拌时,溅出少量溶液 |
E.没有用蒸馏水洗烧杯2—3次,并将洗液移入容量瓶中
F.将量筒洗涤2—3次,并全部转移至容量瓶中
G.容量瓶中原来存有少量蒸馏水
H.胶头滴管加水定容时俯视刻度
某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了下列实验:(1)用如图所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成 高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水和铁反应)。
高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水和铁反应)。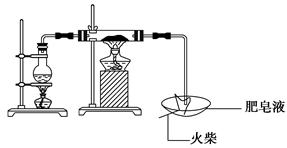
①反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当________时(填实验现象),说明“铁与水蒸气”能够进行反应。
②写出铁与水蒸气反应的化学方程式_______________。
③实验中石棉绒的作用是。
(2)为了研究一定时间内铁粉的转化率,他们设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成气体的体积,计算出铁粉的转化率。
①收集并测量气体体积应选图中的________装置。
②称取0.24 g铁粉与适量石棉绒混合,然后加热至无气体放出。若室温下氢气密度约为0.088 g/L,最好选用______规格的量筒(选填字母序号)。
| A.100 mL | B.200 mL |
| C.500 mL | D.1 000 mL |
实验室需要0.80 mol/L NaOH溶液475 mL和0.40 mol/L硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是___________(填序号),配制上述溶液还需用到的玻璃仪器是________________________(填仪器名称)。
(2)根据计算用托盘天平称取NaOH的质量为_______g;根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为______mL。
(3)下图是某同学转移溶液的示意图,图中的存在的错误是_______________________。
(4)在实验中其他 操作均正确,若定容时俯视视刻度线,则所得溶液浓度_____0.8 mol/L(填“>、<或=”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度_____0.8 mol/L。
操作均正确,若定容时俯视视刻度线,则所得溶液浓度_____0.8 mol/L(填“>、<或=”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度_____0.8 mol/L。
(15分)有甲、乙两个探究性学习小组,他们拟用小颗粒状铝硅合金与足量稀硫酸的反应测定通常状况(约20℃,1atm)下气体摩尔体积的方法。
(1)甲组同学拟选用图27题-l的实验装置完成实验:
①铝硅合金与足量稀硫酸的反应的离子方程式__________________________________。
②该组同学必须选用的装置的连接顺序是A接( )( )接( )( )接( )(填接口字母,可不填满。)
③实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,过一会儿后稀硫酸就不能顺利滴入锥形瓶。请你帮助分析原因_________________________________________
_____________ _______________________________________________________________。
_______________________________________________________________。
④实验结束时,测量实验中生成氢气的体积时应注意:a.待实验装置
冷却到(约20℃,1atm)后,上下移动量筒,使其中液面与广口瓶中
液面相平,b.______________________________________。
(2)乙组同学仔细分析甲组同学的实验装置后,认为:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了图27题-2所示的实验装置。
装置中导管a的作用是
_________________________ ___________________________
___________________________
_____________________________________________________。
②实验中准确测得4个数据:实验前铝硅合金的质量m1g,实验后残留固体的质量m2g,实验前后碱式滴定管中液面读数分别为V1mL、V2mL。则通常状况时气体摩尔体积Vm=_______L·moL-1。