(1)某氯化镁溶液的密度为d g·cm-3,其中镁离子的质量分数为A%,则300 mL该溶液中c (Cl-)= (mol/L)。
(2)无土栽培中,需配制营养液NaH2PO4、Na2HPO4(物质的量之比为4 : 1),已知每升含磷元素0.10mol,现用4.0mol/LH3PO4和固体NaOH配制2 L该营养液需要:
V(H3PO4)= (mL),m(NaOH)= (g)。
(3)甲、乙两烧杯中各成盛有100mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为 甲 : 乙=1 : 2,则加入铝粉的质量为: (g)。
Fe2O3和Cu2O都是砖红色粉末,课外小组通过实验探究某砖红色粉末是Fe2O3、Cu2O或者是二者混合物。探究过程如下:
查阅资料:Cu2O是碱性氧化物,Cu2O与H+反应生成的Cu+不稳定,立即转化成Cu2+和Cu。提出假设:假设1:红色粉末是Fe2O3;假设2:红色粉末是Cu2O;假设3:红色粉末为Fe2O3、Cu2O的混合物
设计探究实验
取少量粉末,向其加入足量稀盐酸在所得溶液中滴加苯酚溶液
(1)若假设1成立,则实验现象是。
(2)若滴加苯酚后溶液不变紫色,则证明原固体粉末不含Fe2O3。你认为结论是否合理(填“合理”或“不合理”),简述理由。
(3)若固体粉末完全溶解无固体存在,滴加苯酚时溶液不变紫色,证明原固体粉末是,相关的离子方程式为。(任写其中一个)
某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向滤液中滴加稀硫酸至溶液的pH=8~9,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4:将得到的溶液蒸发浓缩、冷却、结晶、过滤、干燥。
请回答以下问题
(1)上述实验中的过滤操作需要玻璃棒、______________、______________等玻璃仪器。
(2)步骤1过滤的目的是__________________________________________。
(3)当步骤2中的溶液pH=8~9时,检验沉淀是否完全的方法是____________。
反应①②是重要的化工反应,D、E、F、G为单质,D、E、G、H为气体,且只有E为有色气体,F是常见的金属单质,G是空气中主要成分之一,K是白色胶状沉淀,C的焰色反应为黄色,其物质间的转化关系如下,虚框内是需设计的内容,反应物只能用A~J中的物质: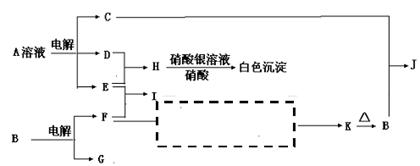
(1)A的电子式, H的结构式是;
(2)A溶液的电解方程式是;
C+B→J的离子方程式是;
(3)请设计F→K的最佳途径
(4)按设计得到1mol K,电解B时转移的电子数目是,至少需要另加试剂的物质的量是:mol,:mol,:mol(可不填满)。
等质量的铜、铁、锌三种金属混合物Ag投入FeCl3与盐酸的混合溶液中,充分反应后:
(1)若无剩余固体,则溶液中的阳离子一定有、可能有。
(2)若剩余固体质量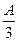 g,则溶液中的阳离子一定有、可能有、一定没有。
g,则溶液中的阳离子一定有、可能有、一定没有。
(3)若剩余固体质量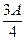 g,则溶液中的阳离子一定有、一定没有。
g,则溶液中的阳离子一定有、一定没有。
2001年1月6日,我国525名两院院士投票评选出1999年中国十大科技进步奖,其中一项是:储氢碳纳米管研究获重大进展。电弧法合成的碳纳米管,常伴有大量杂质——纳米颗粒。这种碳纳米颗粒可用氧化汽化法提纯。 其反应式是3C+2 K2Cr2O7+ 8H2SO43CO2↑+2K2SO4+2Cr2(SO4)3+8H2O
其反应式是3C+2 K2Cr2O7+ 8H2SO43CO2↑+2K2SO4+2Cr2(SO4)3+8H2O
(1)单线法标出电子转移的数目和方向。
(2)此反应的氧化剂是氧化产物是。
(3)H2SO4在上述反应中表现出来的性质是(填选项编号)
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
(4)上述反应中若产生0.1mol气体物质,则转移电子的物质的量是mol.