“NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl”是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是
在密闭容器里,A与B反应生成C,其反应速率分别用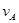 、
、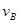 、
、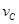 表示,已知2
表示,已知2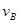 =3
=3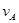 、3
、3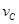 =2
=2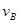 ,则此反应可表示为
,则此反应可表示为
| A.2A+3B=2C | B.A+3B=2C | C.3A+B=2C | D.A+B=C |
已知反应X+Y= M+N为放热反应,,对该反应的下列说法中正确的()
| A.X的能量一定高于M |
| B.Y的能量一定高于N |
| C.X和Y的总能量一定高于M和N的总能量 |
| D.因该反应为放热反应,故不必加热就可发生 |
下列说法不正确的是()
| A.化学反应除了生成新物质外,还伴随着能量的变化 |
| B.放热反应都不需要加热就能发生 |
| C.吸热反应在一定条件(如常温、加热等)也能发生 |
| D.化学反应是放热还是吸热,取决于生成物和反应物具有的各自总能量 |
下列变化属于吸热反应的是()
①液态水汽化②将胆矾加热变为白色粉末③浓硫酸稀释④氯酸钾分解制氧气⑤生石灰跟水反应生成熟石灰
| A.①④⑤ | B.①②④ | C.②③ | D.②④ |
对于可逆反应 A(g) +2B(g) 2C(g)△H>0,下列图像中正确的是
2C(g)△H>0,下列图像中正确的是