Cl2是一种重要的化工原料,结合氯气的相关知识解决下列问题。
(1)运输氯气的钢瓶上应贴的标签为_____________。
| A.腐蚀品 | B.爆炸品 | C.有毒品 | D.易燃品 |
(2)工业上将氯气通入石灰乳制取漂白粉,写出该反应的化学方程式 。
(3)漂白粉的有效成分是(填化学式)_____________。
(4)实验室可以用KMnO4与浓盐酸在常温下制备Cl2。高锰酸钾溶液常用于物质的定性检验与定量分析。某化学兴趣小组在实验室里欲用KMnO4固体来配制500 mL 0.1mol/L的KMnO4溶液。
①需用的仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、 。
②下列操作会导致实验结果偏小的是 (填字母)。
a.转移时没有洗涤烧杯、玻璃棒
b.容量瓶内壁附有水珠而未干燥处理
c.颠倒摇匀后发现凹液面低于刻度线又加水补上
d.加水定容时俯视刻度线
③用配好的该浓度的KMnO4溶液与300mL 0.2mol/L的KI溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的体积为 mL。(已知MnO4-在此条件被还原为Mn2+)
(5)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量,已知:Cl2 + 2Br-=2Cl-+ Br2)。

①能证明氯水具有漂白性的是__________(填“a”、“b”、“c”或“d”),现象是 。
②a中发生反应的离子方程式是 。
实验室采用如下图所示的装置,可将反应粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。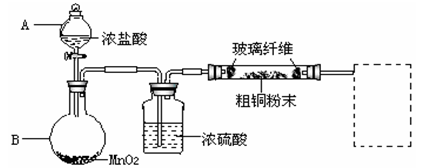
(1)仪器A的名称是 。
(2)连接好装置后,加入药品前,应该进行的实验操作是 。
(3)装置B中发生反应的离子方程式是 。
(4)有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”) 。
(5)虚线内缺少实验装置,请你画出装置图,标明药品名称。
某同学在实验室进行钠的化合物性质的实验。请回答下列问题。
(1)过氧化钠与水反应的化学方程式为 ,实验结束后,向试管所得溶液中滴加酚酞溶液,现是 。
(2)Na2CO3和NaHCO3是两种常见的钠盐。
①下列关于Na2CO3和NaHCO3性质的说法中,正确的是________(填字母)。
a. NaHCO3的俗称是苏打
b. Na2CO3溶液显碱性,说明Na2CO3属于碱
c. 向Na2CO3和NaHCO3固体中分别滴加等浓度的盐酸,后者反应速率快
②按下图所示装置做实验,请回答下列问题。
___________(填“A”或“B”)中澄清石灰水变浑浊,原因是(用化学方程式表示)
________________________________,_________________________________。
某研究性学习小组请你参与“研究铁与水蒸气反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
探究一 设计如图所示装置进行“铁与水蒸气反应”的实验。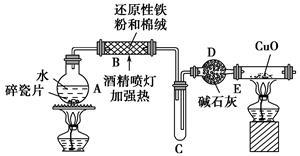
(1)硬质玻璃管B中发生反应的化学方程式为____________________。
(2)反应前A中投放碎瓷片的目的是______________________。
(3)装置E中的现象是___________________________。
探究二 设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于________后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为________(选填序号,下同);若溶液未变红色,推断硬质玻璃管B中固体物质的成分为________。
①一定有Fe3O4 ②一定有Fe ③只有Fe3O4 ④只有Fe
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
|

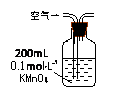
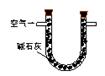
Ⅰ.(1)某兴趣小组甲设计了以下装置和方法测定空气中SO2含量。你认为可行的操作是 (填序号)
| 序号 |
A |
B |
C |
| 装置 |
 |
 |
 |
| 原理 |
通入V升空气,测定生成沉淀的质量 |
当KMnO4溶液刚好褪色时,测定通入空气的体积V |
通入V升空气,测定U型管增加的质量 |
(2)兴趣小组乙取336mL(标准状况)某由SO2和N2组成的混合气体Y,将其通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为 。
Ⅱ某化学兴趣小组丙为探究Fe3+是否能氧化SO2,设计了如下实验装置。
(1)如上图连接好装置。实验前应进行 操作
(2)观察到装置C中产生了白色沉淀,同学们提出了以下猜想(每个猜想只考虑一种物质的氧化性)。
猜想1: ;
猜想2:SO2被Fe3+氧化了;
猜想3:SO2被NO3—氧化了
(3)甲同学认为猜想1正确,并利用上述装置A进行了排除干扰的探究实验。
(4)乙同学认为猜想2正确,则装置C中反应的离子方程式是
(5)丙同学认为猜想3正确,他利用甲同学的实验装置,设计实验验证猜想。请在表格中写出实验步骤以及预期现象和结论。限选实验试剂:NaNO3溶液、KSCN溶液、FeCl3溶液、BaCl2溶液、Fe(NO3)3溶液
| 实验步骤 |
预期现象和结论 |
关于电解池应用的规律提炼题组
某化学兴趣小组用下图所示装置进行电化学原理的实验探究,回答下列问题:
(1)通O2的Pt电极为电池 极(填电极名称),其电极反应式为 。
(2)若B电池为电镀池,目的是在某镀件上镀一层银,则X电极材料为 ,电解质溶液为 。
(3)若B电池为精炼铜,且粗铜中含有Zn、Fe、Ag、Au等杂质,在 电极(填“X”或“Y”)周围有固体沉积,该电极的电极反应式为 。
(4)若X、Y均为Pt,B电池的电解质溶液为500 mL 1.0mol/L的NaCl溶液,当电池工作一段时间断开电源K,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全溢出,溶液体积不变)。恢复到常温下,B电池溶液的pH= ,要使该溶液恢复到原来的状态,需加入 (填物质并注明物质的量)。
(5)若X、Y均是铜,电解质溶液为NaOH溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是Cu2O,试写出该电极发生的电极反应式为 。
(6)若X、Y均是Pt,电解质溶液为Na2SO4溶液,通电一段时间后,在阴极上逸出c mol气体,同时有N g Na2SO4•10H2O 晶体析出,若温度不变,此时剩余溶液的溶质的质量分数为 。
(学法题)通过以上题目,请总结书写电极反应式的关键 。