为探究铁和稀硝酸反应的产物,某兴趣小组进行如下实验。
查阅资料
i.NO+Fe(NO)SO4(棕色)
ii.KMnO4溶液可氧化吸收NO和NO2
iii.0.2mol∙L-1NaOH溶液可完全吸收NO、NO2混合气体中的NO2,而不吸收NO
实验Ⅰ 用以下装置验证铁和过量12mol∙L-1硝酸反应产生的气体中含有NO

(1)图1的A装置中加入硝酸前需加入N2一段时间的目的是______________。
(2)通N2一段时间后,加入12mol∙L-1硝酸后看到A装置中产生红棕色气体,B装置中溶液变棕色。根据实验现象不能确定产生的气体中含有NO,理由是_______________。请在图1装置的基础上提出改进措施______________________。
(3)用图1的A装置和图2装置可测量反应产生的NO体积,实验操作如下
a.连接装置,并检查气密性
b.往A装置中加入铁片后,再往分液漏斗加入12mol∙L-1的硝酸
c.通N2一段时间后关闭
d.向水槽中加入0.2 mol∙L-1NaOH溶液
e.打开分液漏斗活塞,加入一定量12 mol∙L-1硝酸后,关闭活塞
f.将装满0.2 mol∙L-1NaOH溶液的量筒倒扣在水槽中
g.待反应装置恢复至室温时,读取数据
①操作的正确顺序是a→b→______→______→______→______→g
②读取数据时应注意__________________。
实验Ⅱ 对4mol∙L-1硝酸与过量铁反应的产物进行探究
反应过程中溶液中c(H+)和产生气体的体积(标准状况下)随铁的消耗量变化关系如下图所示。
(4)据图推测HNO3在bc段的还原产物是_________(填化学式);若在ab段只产生单一的气体,则该气体是________(填化学式)。

钢铁工业是国家工业的基础,是日常生活中用途最广、用量最大的金属材料。
(1)常温下,可用铁质容器盛装浓硫酸的原因是。
(2)在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,俗称“引火铁”。请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6mol/L盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。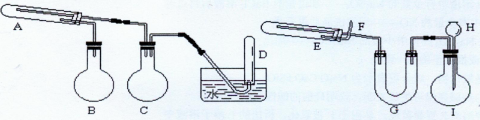
填写下列空白:
①实验进行时试管A中应加入的试剂是;烧瓶B的作用是;烧瓶C的作用是。
②实验时,U型管G中加入的试剂是;长颈漏斗H中应加入。
③试管E中发生反应的化学方程式是。
④为了安全,在E管中的反应发生前,在F出口处必须。
为了探究Cl2、SO2同时通入H2O发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。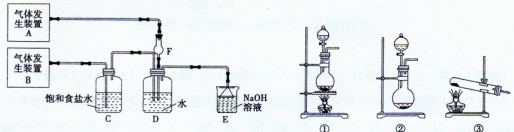
试填空:
(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12 mol·L-1)为原料制取Cl2。在此实验中,F仪器的作用是;气体发生装置B应选择①、②、③三种装置中的(选填序号)。
(2)D装置中主要反应的离子方程式为:。
(3)为验证通入D装置中气体是Cl2过量还是SO2过量,兴趣小组的同!学准备了以下试剂:氯化铁溶液;氯化亚铁溶液;硫氰化钾溶液;苯酚溶液;品红溶液;酸性高锰酸钾溶液。
若Cl2量:取适量D中溶液滴加至盛有(试剂名称,下同)的试管中,再加入产生的现象是,说明Cl2过量;
若SO2过量:取适量D中溶液滴加至盛有的试管内,产生的现象是。
某强酸性溶液X中含有Ba2+、Al3+、SiO32-、NH4+、Fe2+、Fe3+、CO32-、SO42-、NO3-中的一种或几种离子,取该溶液进行连续实验,能实现如下转化: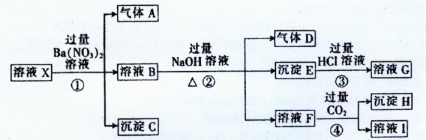
根据以上信息,请同答下列问题:
(1)上述离子中,溶液X肯定含有的离子是,不能确定是否含有的离子是。
(2)气体D的化学式为,,沉淀E的化学式为,沉淀H的化学式为。
(3)反应①、②、③、④中,属于氧化还原反应的是(填序号)。
碘在工农业生产和日常生活中有重要用途。
(1)右图为海带制碘的流程图。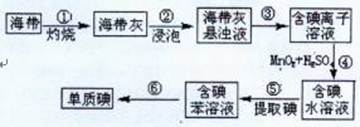
步骤③和⑤的实验操作名称分别是、;
步骤④中发生反应的离子方程式为;
若步骤⑤采用四氯化碳来提取碘,将四氯化碳加入含碘水溶液中并振荡,观察到的现象是。
(2)把滤纸用淀粉和碘化钾溶液浸泡,晾干后就是实验室常用的淀粉碘化钾试纸。利用淀粉碘化钾试纸可检验具有某种特性的气体。你认为淀粉碘化钾试纸用于检验具有的气体(填序号)
| A.酸性 | B.碱性 | C.氧化性 | D.还原性 |
理由是。
(16分)纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
(1)制备纳米TiO2的方法之一是TiCl4水解生成TiO2·x H2O,该水解反应的化学方程式为。再经过滤、水洗除去其中的Cl–,再烘干、焙烧除去水分得到粉体TiO2。检验TiO2·xH2O中Cl–是否被除净的方法是。
(2)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
①配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是;
②滴定终点的现象是。
③滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为。
④下列操作对TiO2质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”)
若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果。
若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果。