合理使用药物是保证身心健康、提高生活质量的有效手段。药物化学已经成为化学的一个重要领域。
(1)我国科学家屠呦呦因发现治疗疟疾的特效药——青蒿素,而获得2015年诺贝尔生理学或医学奖。青蒿素的结构简式如右图所示,其含有的过氧基(—O—O—)具有强氧化性。

请回答下列问题:
①青蒿素的分子式为_______________________。
②下列有关青蒿素的叙述中,正确的是__________(填字母)。
A、青蒿素属于芳香族化合物
B、青蒿素具有强氧化性,可用于杀菌
C、青蒿素分子中的所有碳原子在同一个平面上
D、在一定条件下,青蒿素能与NaOH溶液发生反应
(2)阿司匹林(乙酰水杨酸) 是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为:
是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为:

请回答下列问题:
①乙酰水杨酸中的含氧官能园的名称为____________________。
②制得的阿司匹林中常含有少量的杂质水杨酸,下列试剂可用于检验阿司匹林样品中是否混有水杨酸的是________________(填字母)。
A、碳酸氢钠溶液 B、三氯化铁溶液 C、石蕊试液
③写出水杨酸与足量的NaHCO3溶液完全反应所得有机产物的结构简式:_____________。
④1 mol乙酰水杨酸与足量的NaOH溶液反应,最多消耗NaOH物质的量为_________mol。
某同学用铁、铜作为电极,稀硫酸作为电解液组成原电池,如图所示,完成下列空格。
(1)正极是 (填“铜极”或“铁极”),现象是:,电极反应是: ,发生反应(填“氧化”或“还原”)。
(2)电流从经导线流到(填“铜极”或“铁极”)。
(3)若反应生成的氢气在标况下为4.48L,则反应过程中有mol电子发生转移,溶解的铁质量为g。
在下列中学化学中常见物质的转化关系图中,已知常温下A为淡黄色固体、B为金属单质,D、E、M是常见气体单质,其中M为黄绿色,N是胃酸主要成分,工业上用E和M来制取N,试推断: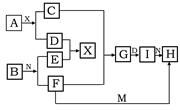
(1)写出下列化学式 AI
(2)G转化为I的现象为
(3)F+M→H离子方程式为
(4)A+X→C+D的化学方程式为________________________
①②③④⑤五种元素,在元素周期表中的位置如图所示。回答下列问题: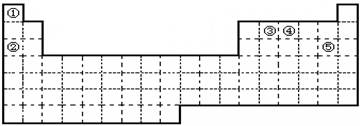
(1)上述五种元素中,金属性最强的元素在周期表中的位置是,
该元素的单质在空气中加热的化学方程式为。
(2)元素①和④形成化合物的电子式是,其水溶液呈(填“碱性”、“酸性”或“中性”)。
(3)试用电子式表示元素⑤单质分子的形成过程。
(1)对可逆反应aA(g)+bB(g) cC(s)+dD(g)达到平衡时,其反应的K值与温度有关。请写出该反应的平衡常数表达式
cC(s)+dD(g)达到平衡时,其反应的K值与温度有关。请写出该反应的平衡常数表达式
现有反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0。在850 ℃时,K=1。
CO2(g)+H2(g) ΔH<0。在850 ℃时,K=1。
(2)若升高温度到950 ℃,达到平衡时K________1(填“大于”“小于”或“等于”)。
(3)850 ℃时,若向一容积可变的密闭容器中同时充入1.0 mol CO、3.0 mol H2O、1.0 mol CO2和x mol H2
①当x=5.0时,上述平衡向________(填“正反应”或“逆反应”)方向移动。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是________________。
汽车内燃机工作时产生的高温会引起N2和O2发生反应:N2(g)+O2(g) 2NO(g),这是汽车尾气中含有NO的原因之一。某同学为探究控制污染的方法,对该反应进行研究。
2NO(g),这是汽车尾气中含有NO的原因之一。某同学为探究控制污染的方法,对该反应进行研究。
(1)如图表示在T1、T2两种不同温度下,一定量的NO发生分解过程中N2的体积分数随时间变化的图象。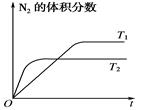
①达到平衡后反应速率v1(T1条件下)________v2(T2条件下)(填“>”、“<”或“=”)。
②N2(g)+O2(g) 2NO(g)为________(填“吸热”或“放热”)反应。
2NO(g)为________(填“吸热”或“放热”)反应。
(2)为避免汽车尾气中的有害气体对大气造成污染,应给汽车安装尾气净化装置。净化装置里装有含Pd等过渡元素的催化剂,写出CO、NO在催化剂作用下转化为无害气体的化学方程式: