下列叙述正确的是
| A.NaCl的摩尔质量是58.5g |
| B.将40g氢氧化钠溶解在1L水中可配制物质的量浓度为1mol/L的氢氧化钠溶液 |
| C.气体摩尔体积指lmol任何气体所占的体积约为22.4L |
| D.10毫升1mol/L氯化铝溶液与50毫升3mol/L氯化钠溶液中所含氯离子物质的量浓度相等 |
设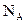 为阿伏加德罗常数的值,下列叙述中正确的是( )
为阿伏加德罗常数的值,下列叙述中正确的是( )
A.92 g NO2和N2O4混合气体中含有的分子数为2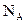 |
B.标准状况下,11.2 L SO3中含有的电子数为20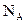 |
C.0.5 mol·L-1的Ba(OH)2溶液中OH-的数目为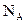 |
D.1 mol Mg与足量的O2或N2反应生成MgO或Mg3N2时,失去的电子数均为2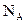 |
下列各组离子加入足量的氨水后,现象有明显不同的是( )
①Al3+、Fe3+
②Al3+、Cu2+
③K+、Ba2+
④Mg2+、Al3+
⑤Fe3+、Fe2+
| A.①②⑤ |
| B.①②④⑤ |
| C.①②④ |
| D.③④⑤ |
某化学兴趣小组为测定Fe、Cu、Ag三种金属的活动性顺序设计了四种方案,每种方案所需试剂如下,你认为不可行的是( )
| A.Fe、Ag、CuSO4溶液 |
| B.Cu、Ag、FeSO4溶液 |
| C.Fe、Cu、稀盐酸、AgNO3溶液 |
| D.Cu、FeC l2溶液、AgNO3溶液 |
2005年10月12日,载有两名航天员的“神舟”六号在酒泉发射中心顺利升空并于5天后安全返回,这表明我国的载人航天事业又取得新的突破。下图是“神六”发射升空时的照片。推动上千吨的火箭和飞船的巨大能量是从哪里来的?化学反应立下神功。火箭使用的燃料是偏二甲肼〔(CH3)2NNH2〕,火箭升空时发生的化学反应为:C2H8N2+2N2O4====2CO2↑+3N2↑+4H2O↑。下列有关该反应的说法正确的是( )
| A.该反应的氧化剂是偏二甲肼 |
| B.该反应进行时只有放热过程没有吸热过程 |
| C.该反应中氮元素的化合价升高 |
| D.该反应中每生成1 mol CO2转移8 mol电子 |
下列叙述正确的是( )
| A.同主族金属的原子半径越大,熔点越高 |
| B.稀有气体原子序数越大沸点越高 |
| C.分子间作用力越弱分子晶体的熔点越低 |
| D.同周期元素的原子半径越小越易失去电子 |