研究性学习小组进行了一系列化学实验后,发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,且锰化合物的还原产物都是MnCl2.他们将6.32gKMnO4粉末加热一段时间,也不知道高锰酸钾是否完全分解,收集到0.112L气体后便停止加热了,冷却后放入足量的浓盐酸再加热,又收集到气体体积是(上述气体体积都折合成标准状况)
| A.0.448L | B.2.240L | C.2.016L | D.无法确定 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X>Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
| D.Cs和Ba分别位于第六周期IA和ⅡA族,碱性:CsOH >Ba(OH)2 |
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)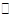 4NO2 +O2(g)△H>0,T1温度下的部分实验数据为:
4NO2 +O2(g)△H>0,T1温度下的部分实验数据为:
| t/s |
0 |
500 |
1000 |
1500 |
| c(N2O5)mol/L |
5.00 |
3.55 |
2.50 |
2.50 |
下列说法中,正确的是:
A.当反应体系内气体的平均相对分子质量不再发生变化时则该反应达到了平衡
B.T1温度下的平衡常数为K1=125,500s时N2O5的转化率为71%:
C.其他条件不变时,T2温度下反应到2000s时测得N2O5 (g)浓度为2.78mol/L, 则T1<T2
D.T1温度下的平衡常数为K1,若维持T1温度不变,增加体系压强,达到新的平衡时,平衡常数为K2,则K2>K1
设NA为阿伏加德罗常数的数值,下列说法中正确的是
| A.电解精炼粗铜时,每转移NA个电子,阳极溶解32g铜 |
| B.1L0.1mo1·L-1的氨水中含OH-离子数为0.lNA个 |
| C.常温常压下,a mo1O2与2a mo1NO混合,降温得到混合气体中氧原子数小于4aNA |
D.在反应5NH4NO3 2HNO3+4N2↑+9H2O中,每生成4molN2,转移电子数为15NA 2HNO3+4N2↑+9H2O中,每生成4molN2,转移电子数为15NA |
化学与生产、生活密切相关。下列叙述正确的是
| A.PM2.5的产生与人类活动无关 |
| B.苏丹红、三聚氰胺、地沟油、生石灰粉都属于对人体有害的有机物 |
| C.14C可用于测定一些文物的年代,12C与14C互为同位素 |
| D.明矾可用于水的消毒、杀菌 |
在一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g) 2C(g) △H<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图。下列说法正确的是
2C(g) △H<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图。下列说法正确的是
| A.0~t2时,v正>v逆 |
| B.t2时刻改变的条件可能是加催化剂 |
| C.Ⅰ、Ⅱ两过程达到反应限度时,A的体积分数Ⅰ=Ⅱ |
| D.Ⅰ、Ⅱ两过程达到反应限度时,平衡常数I<Ⅱ |