一次用餐中,小丽对"固体酒精"产生好奇,于是她买回一袋,和同学一起对其进行研究.
【查阅资料】固体酒精中含有酒精、氢氧化钠等物质.
【提出问题】固体酒精中的氢氧化钠是否变质及变质的程度如何?
【提出猜想】小丽猜想:没有变质,只含有氢氧化钠.
小明猜想:全部变质,只含有碳酸钠.
你的猜想:部分变质,含有 .
氢氧化钠在空气中变质的化学方程式 .
【实验探究】小丽取少量固体酒精在水中充分溶解后过滤,取上述滤液于试管中,滴入几滴稀盐酸,无明显现象;小丽说氢氧化钠没有变质,小明认为她的结论不正确,其理由是 .
请你补全实验设计,填写表格中的①②③,证明固体酒精中氢氧化钠是否变质及变质的程度如何.
实验操作 |
实验现象 |
实验结论 |
① |
有气泡产生 |
小丽猜想不成立 |
② |
③ |
你的猜想成立 |
【拓展应用】除去部分变质的氢氧化钠溶液中的杂质,方法是 (用化学方程式表示).
我市著名的纸面石膏板企业,用热电厂燃烧煤产生的炉渣来生产石膏板.原理是:发电过程中产生的烟气中含有大量的SO 2,热电厂用"碱﹣石灰﹣石膏(CaSO 4•2H 2O)"的方法使烟气脱硫从而生成石膏.
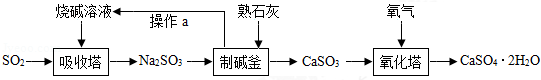
(1)工业烟气没经处理直接排放到空气中易形成 ,会污染、破坏环境;
(2)写出吸收塔内发生反应的化学方程式 ;工业上用分离液态空气法制氧气,是利用空气中各成分的 不同进行分离的;
(3)化学反应类型有不同的分法,其中反应前后,有元素化合价变化的化学反应是氧化还原反应.有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂.化学反应前后元素化合价没有变化的化学反应是非氧化还原反应.则下列说法正确的是
A、吸收塔、制碱釜中发生反应属于氧化还原反应
B、制碱釜中的反应物Na 2SO 3作氧化剂
C、氧化塔中发生的反应属于氧化还原反应
D、氧化塔中的反应物CaSO 3作还原剂
(4)生产流程中生成的 可循环利用,节约成本.
实验技能是学习化学和进行探究活动的基础和保证。

(1)实验室配制50g质量分数为6%的NaCl溶液,用到的玻璃仪器除试剂瓶、量筒、胶头滴管外,还需要 。量取读数时,如图视线角度正确的是 (填序号)。
(2)请根据如图装置或操作回答相关问题。
①选取图2中的序号,表示粗盐提纯的正确操作顺序为 。操作B的名称是 ,该操作中当 时,应停止加热。
②实验室用高锰酸钾固体制取氧气时,可选用的发生装置是 (填序号)。
铅蓄电池在生产、生活中使用广泛。其构造示意图如图1,回答下列问题:

(1)铅蓄电池充电时是将电能转化为 (填序号)。
a、机械能 b、热能 c、化学能
(2)铅蓄电池放电过程中,反应的化学方程式为Pb+PbO 2+2H 2SO 4═2PbSO 4+2H 2O,据此可知,铅蓄电池在放电时,溶液的pH不断 (填"增大"、"减小"或"不变")。
(3)如图2是回收废铅蓄电池的一种工艺流程:
①从材料分类角度看,塑料是一类 材料。
②废硫酸可以与氟磷灰石[Ca 5(PO 4) 3F]反应,反应的化学方程式为2Ca 5(PO 4) 3F+7H 2SO 4═3CaSO 4+3Ca(H 2PO 4) 2+2HF,反应产物中可用作化肥的物质是 。
③如表是一些金属熔点的数据:
|
金属 |
锡 |
铅 |
铋 |
镉 |
|
熔点∕℃ |
231.9 |
327.5 |
271.3 |
320.9 |
日常所用保险丝由铋、铅、锡、镉等金属组成,其熔点约为 (填序号)
A.300﹣320℃
B.230﹣250℃
C.60﹣80℃
D.20﹣40℃
④废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
|
物质 |
CaCO 3 |
Ca(OH) 2 |
NH 3 |
NaOH |
|
市场参考价(元/kg ) |
1.8 |
2.0 |
6.5 |
11.5 |
已知:2NH 3+H 2SO 4═(NH 4)SO 4,如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择 (填序号)。
a、CaCO 3 b、Ca(OH) 2c、NH 3d、NaOH。
金属在日常生活,工农业生产和科学研究方面应用广泛.
(1)铜可用来制作导线,是因为其具有良好的延展性和 .
(2)在空气中,铝表面生成一层致密的氧化膜,氧化膜的主要成分是 .
(3)某实验小组为了探究影响金属与酸反应快慢的因素,进行如表实验
|
实验序号 |
实验过程 |
实验现象 |
|
1 |
镁粉和铁粉分别与5%盐酸反应 |
镁粉产生气体快 |
|
2 |
铁粉和铁片分别与15%盐酸反应 |
铁粉产生气体快 |
|
3 |
铁片分别与5%盐酸和15%盐酸反应 |
15%盐酸产生气体快 |
由此得出影响金属与酸反应快慢的因素有:
a: b: c:
(4)小明将一包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液.
①锌和硝酸银溶液反应的化学方程式是 .
②若滤液为蓝色,则滤液中一定含有的金属离子是 (写离子符号)
PLA是一种新型可降解塑料,能有效缓解塑料垃圾造成的白色污染。已知PLA由碳、氢、氧三种元素组成,为了测定7.2gPLA样品氧元素的质量,某化学兴趣小组进行了以下探究。
【实验设计】查阅资料,无水硫酸铜遇水由白色变成蓝色

将7.2gPLA样品充分燃烧,为分别吸收燃烧产物并通过清晰可见的现象检验吸收是否完全,以上实验装置正确的连接顺序是:A→ → → → (填写装置的字母序号)。
【分析与结论】①实验中选择纯净的氧气而不用空气的原因是 。
②装置E的作用是 。
③正确连接装置后,确认气密性良好。充分燃烧7.2gPLA样品,测得相关实验数据见下表(已知燃烧产物被完全吸收,灰烬质量忽略不计)。
通过分析与计算,可知7.2gPLA样品中含有氧元素的质量为 克,该PLA样品中碳、氢、氧三种元素的原子个数最简整数比为 。
|
装置 |
B |
C |
D |
E |
|
实验前质量/g |
160 |
150 |
150 |
100 |
|
实验后质量/g |
163.6 |
150 |
163.2 |
100 |