钙是维持人体正常功能所必需的元素,葡萄糖酸钙(C 12H 22O 14Ca)是人们常用的一种补钙剂(已知葡萄糖酸钙的相对分子质量是430)。
(1)葡萄糖酸钙中碳、氧元素质量比为 (填最简比);
(2)要补充0.8g钙元素,则需葡萄糖酸钙的质量为 g。
工业上常用电解饱和氯化钠水溶液的方法制备氢氧化钠,化学方程式为
2NaCl+2H2O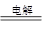 2NaOH+Cl2↑+H2↑。若制得16.0g氢氧化钠,可同时得到氯气的质量是多少?
2NaOH+Cl2↑+H2↑。若制得16.0g氢氧化钠,可同时得到氯气的质量是多少?
某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答: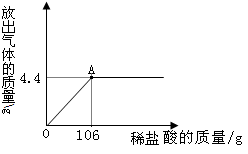
(1)当加入212g稀盐酸时,放出气体的质量为__________g
(2)碳酸钠样品中碳酸钠的质量分数为多少?(写出计算过程)
(3)加入106g稀盐酸(即A点)时烧杯中溶液溶质的质量分数为多少?(写出计算过程)
“过碳酸钠”(2Na2CO3·3H2O2)俗称固体双氧水,它既有碳酸盐的性质,又有双氧水的不稳定性和氧化性,是很好的消毒剂和供氧剂,广泛应用于洗涤、印染和医药等领域。“过碳酸钠”的制备流程如下: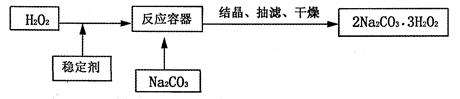
请回答下列问题:
(1)H2O2在催化或受热条件下易分解,说明化学变化的速度和相关;
(2)在“过碳酸钠”中加入下列物质时,不会导致“过碳酸钠”变质的是(填序号)。
| A.二氧化锰 |
B.稀盐酸 |
C.硫酸钠 |
D.石灰水 |
(3)“过碳酸钠”极易分解,得到碳酸钠、水和氧气,其反应方程式可表示为
2(2Na2CO3.3H2O2)==4Na2CO3+6H2O+3O2↑
请通过计算说明(必须有计算的过程):
①若“过碳酸钠”分解产生氧气12g,则同时产生碳酸钠的质量是多少?
②若将上述产生的碳酸钠全部配制成溶质质量分数为10.6%的溶液,共需水多少毫升?
某同学为了测定NaCl和MgCl2固体混合物中MgCl2的质量分数,进行如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相同质量分数的NaOH溶液,获得如下实验数据:
| 实验次数 |
一 |
二 |
三 |
四 |
| 固体混合物的质量(g) |
20 |
20 |
20 |
20 |
| 加入NaOH溶液的质量(g) |
20 |
40 |
60 |
80 |
| 生成沉淀的质量(g) |
2.9 |
m |
8.7 |
8.7 |
问:(1)表中m的值为;
(2)原固体混合物中MgCl2的质量分数是多少?(要求写出计算过程)
某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图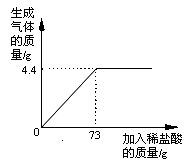
(1)纯碱恰好完全反应时,生成CO2的质量为g
(2)计算该样品中含杂质的质量分数是多少?(计算结果保留一位小数,下同)
(3)计算当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数是多少?