A~F是初中化学常见的物质。各物质之间的相互关系如图所示,图中"→"表示转化关系(部分反应物、生成物、反应条件已略去)。已知A是大理石的主要成分,F只含两种元素。请用初中所学化学知识回答下列问题: 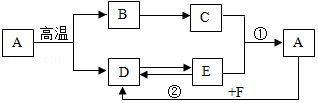
(1)写出C在农业生产中的用途: 。
(2)写出固态D的名称: 。
(3)写出反应①所属的基本类型: 。
(4)写出反应②的化学方程式: 。
将12.5g混有二氧化锰的氯酸钾固体加热至质量不再减少,冷却后称量固体的质量为7.7g。
(1)反应时生成氧气的质量为 g。
(2)计算反应前固体中二氧化锰的质量分数(要求写出计算过程)。
了解常见物质重要的物理及化学性质,有利于我们系统地学习并应用知识解决问题。碱石灰是氧化钙和氢氧化钠固体的混合物,常用来干燥某些气体。某化学兴趣小组的同学对放置在空气中一段时间的碱石灰产生了探究兴趣。
[实验步骤]
步骤一:现将放置在空气中一段时间的碱石灰放入烧杯中,加足量水溶解,烧杯底部有白色沉淀生成;
步骤二:一段时间后过滤,取滤液,加入一定量的碳酸钠溶液,发现没有白色沉淀生成。
据此信息请你参与探究完成下列问题:
[实验探究]
(1)碱石灰中的氧化钙可做某些气体干燥剂的原因是 (用化学方程式表示)。
(2)步骤一向烧杯内的样品加足量的水溶解时,产生的白色沉淀是 。
[实验反思]
(3)固体氢氧化钠曝露在空气中,容易吸收空气中的水分而潮解;同时吸收空气中的 而变质,因此氢氧化钠固体必须密封保存。
(4)综合以上信息,向烧杯内的样品加足量的水溶解时,溶液中溶质组成的情况可能有 (有几种情况就写几种,用化学式表示)。
现有含氯化钠杂质的碳酸钠样品,取6.95g样品溶于水,配制成52.2g溶液。此溶液与50g某溶质质量分数的盐酸恰好完全反应,得到100g溶液。请分析计算:
(1)生成二氧化碳的质量是 。
(2)所得溶液中溶质的质量分数(写出计算过程)。
配制50.0g质量分数为4%的氯化钠溶液,所需氯化钠的质量为 g;水 mL(水的密度为1.0g/mL),量取所需的水需选用 mL的量筒(填"10""50"或"100")。将配制好的50.0g质量分数为4%的氯化钠溶液全部用来在农业上选种(氯化钠溶液的质量分数为16%),最简单的方法是 。
某兴趣小组发现,上周做实验用的氢氧化钠固体忘记了盖瓶盖,他们欲对该固体的变质情况进行探究。
[提出问题]该瓶氢氧化钠固体是否变质,变质情况如何?
[查阅资料]①碳酸钠溶液的pH最大约为10.6,饱和的碳酸氢钠溶液pH约为8.0,氯化钙溶液呈中性。
②NaOH、Na 2CO 3分别在水和酒精中的溶解度如下表所示:
|
物质种类 |
NaOH |
Na 2CO 3 |
|||
|
温度 |
20℃ |
40℃ |
20℃ |
40℃ |
|
|
溶剂 |
水 |
109g |
129g |
21.8g |
49g |
|
酒精 |
17.3g |
40g |
不溶 |
不溶 |
[作出猜想]猜想Ⅰ:固体未变质;猜想Ⅱ:固体部分变质;猜想Ⅲ:固体全部变质。
[实验探究](1)兴趣小组同学取少量样品于烧杯中,加适量水溶解,测得溶液的pH约为12.由此他们得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是 。
(2)组内其他同学取步骤(1)烧杯中少量溶液于试管中,加入过量的 溶液,振荡,有白色沉淀生成;不再产生沉淀时,取上层清液于另一支试管中,滴加 ,溶液变红。
[实验结论]通过实验,兴趣小组证明猜想 正确。
[反思评价]根据查阅资料,有同学提出可以通过氢氧化钠和碳酸钠在酒精中溶解度不同来验证猜想Ⅲ正确。请你帮助他设计实验方案: 。
[实验拓展]实验室使用pH传感器来测定Na 2CO 3和NaHCO 3混合物中NaHCO 3的含量。称取一定量样品,溶于水配成250.0mL溶液。将pH=1的稀盐酸逐滴加入体积为25.0mL的该溶液中,所得曲线如图所示:

a.上一个计量点前发生反应的化学方程式为 。
b.下一个计量点时溶液中大量存在的阴离子是 。