某校实验室有一无色澄清废液,其中除了硝酸钠溶液以外,可能还含有氢氧化钠、碳酸钠、硫酸钠、硝酸钡中的一种或几种。
实验活动一:探究该废液的组成。
取一定量的无色废液,进行如图所示实验。
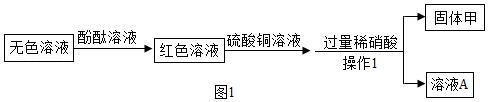
请回答下列问题:
(1)原无色废液呈 (填“酸性”“碱性”或“中性”),操作Ⅰ的名称为 。
(2)生成固体甲的化学方程式为 。
(3)原无色澄清废液中一定没有(写名称或化学式均可,下同) 。
实验活动二:处理废液得到较纯净的硝酸钠溶液。
将溶液A和原无色废液充分混合,无明显现象,接下来进行如图2所示实验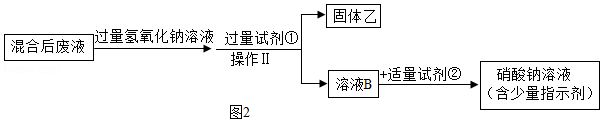
(4)混合后废液中一定含有的溶质是(指示剂除外) ,试剂①是 。
“低碳生活,绿色出行”。如图为沈阳市推广使用的共享单车。请回答下列问题:
(1)自行车的有些部件是由钢铁制成的,请写出用一氧化碳与氧化铁反应来炼铁的化学方程式: 。
(2)为防止自行车链条生锈,可采取的措施是 。
(3)请你从化学的角度写出推广使用共享单车的好处: (答一点即可)。
(4)将一定质量的锌和银投入含有Cu(NO3)2和Fe(NO3)2的混合溶液中,充分反应后过滤,若滤液中只含有一种溶质,则滤渣中一定含有 。

化学就在我们身边,化学与生活息息相关。
(1)某服装标签上写着“涤纶56% 棉44%”,其中属于合成纤维的是 ;生活中常用 方法鉴别棉纤维和羊毛纤维。
(2)煤、 和天然气都属于常见的化石燃料。煤燃烧时排放出二氧化氮、 等污染物,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨。
(3)近阶段经常出现雾霾天气,雾霾的形成原因除了气候因素外,煤、汽油和柴油燃烧时产生的 等排放到空气中形成浮尘也是重要原因。
某氯化钠样品中含有少量氯化镁,取25.8g该样品于烧杯中,加入80克水全部溶解,再加入100克氢氧化钠溶液,恰好完全反应后过滤,得到滤渣5.8克,求:
(1)25.8克该样品中氯化镁的质量;
(2)恰好完全反应后,所得溶液中溶质的质量分数.
对比、归纳是化学学习的重要方法,请补充完成下列实验报告.
【实验目的】探究物理变化和化学变化
【实验过程】
|
实验操作 |
实验现象、分析或结论 |
|
|
实验一 |
步骤一:取少量硫酸铜晶体放在研钵内观察 |
现象:晶体为蓝色 |
|
步骤二:用研杵将硫酸铜晶体研碎. |
现象: . |
|
|
步骤三:在2支试管中分别放入少量研碎前、后的硫酸铜晶体,并加入少量水,振荡得到澄清的硫酸铜溶液. |
现象:研碎后的硫酸铜晶体溶解的更快. 分析:原因是 . |
|
|
步骤四:向上述两支试管中各滴加少量氢氧化钠溶液. |
现象:2支试管中均有蓝色不溶物生成. 分析:(1)该反应的化学方程式是 ; (2)该对比实验得出的实验结论是 . |
|
|
实验二 |
用木炭还原氧化铜 |
现象:有部分黑色粉末变红,澄清石灰水变浑浊. 分析: (1)粉末由黑色变成红色的过程中发生化学反应的化学方程式是 ; (2)上述现象说明木炭和氧化铜发生了化学变化. |
【实验结论】有其他物质生成的变化叫做化学变化,没有其他物质生成的变化叫做物理变化.
如图是实验室常用仪器,利用这些仪器可完成多个实验,请据图回答问题.

(1)加热液体:需要用到的仪器D的名称是 ;
(2)过滤液体:除玻璃棒外,还需选择仪器G、H和 (填字母序号);
(3)制取气体:实验室制取二氧化碳的化学方程式是 ,组装制取并收集二氧化碳的装置,需从上述仪器中选择 (填字母序号).实验室用高锰酸钾制取氧气的化学方程式是 ,利用上述仪器组装发生装置,需要用到的仪器是 (填字母序号).
(4)小杨用澄清的石灰水检验二氧化碳,其原理是 (用化学方程式表示),实验中,小杨观察到石灰水中持续出现气泡,但石灰水始终不变浑浊,你认为可能的原因是 .