科学探究可以培养学生良好的科学思维,某兴趣小组进行了金属燃烧实验:
实验 |
1 |
2 |
3 |
步骤 |
将一片铝箔在空气中用酒精灯加热 |
将另一片相同铝箔伸入到充满氧气的集气瓶中,引燃 |
将一段镁条在空气中用酒精灯加热 |
现象 |
铝箔不燃烧,熔化后也不滴下,外面立即形成一层薄膜 |
铝箔剧烈燃烧,发出耀眼白光 |
镁条剧烈燃烧,发出耀眼白光 |
试回答下列问题:
(1)进行1、2实验的目的是为研究铝和氧气反应的剧烈程度是否与氧气的 有关。
(2)某同学分析1、3实验后就得出了如下结论:不同金属的活动性是不同的,其他同学认为这个结论不可靠,你认为他们的理由是 。
(3)在实验1中,有同学用细针去刺破液态铝外的薄膜。观察到里面的液体铝依然没有流出来,实验后,同学们查阅资料获知该薄膜是氧化铝,其熔点明显高于酒精灯火焰的温度,由此推断,刺破薄膜后液态铝会迅速和 反应又会形成致密氧化膜,所以液态铝不会流出来。
天然气作为燃料已进入千家万户。小聪在帮助父母烧菜时想到:天然气燃烧的产物是什么呢?带着这一问题,小聪和同学一起进行了如下的探究。
(1)设计与实验:同学们设计了甲图装置(固定装置未画出),将天然气在氧气中点燃后得到的混合气体通过该装置进行实验。开始时应______(填“先通气体”或“先加热”);加热过程中发现黑色CuO固体变红,澄清石灰水变浑浊。写出CuO固体变红的化学方程式__________________。仅根据甲图装置出现的现象,写出混合气体所有的可能组成____________。
(2)评价与改进:小聪认为上述实验方案有缺陷,通过讨论,增加了乙图中的3个装置(固定装置未画出),对方案作了改进并进行实验:将混合气体先通过乙图中连接的装置后,再通入甲图装置。实验中部分现象如下:A装置质量增加,B装置中溶液不变浑浊,甲图装置中实验现象与(1)相同。
请你写出改进方案的装置连接顺序(装置不重复使用):混合气体→______→甲图装置(填装置编号)。
(3)交流与讨论:通过对改进实验的现象分析,同学们得出了正确的结论。
张宁和刘明同学学习完酸、碱、盐后发现:碱溶液能使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红。通过学习知道,碱溶液使酚酞溶液变红,是因为碱在水中离解出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞溶液变红呢?请你帮助他俩完成实验探究。
【提出问题】Na2CO3属于 (填“酸”、“碱”、“盐”),为什么能使酚酞溶液变红?
【进行猜想】
(1)Na+使酚酞溶液变红。
(2)水分子使酚酞溶液变红。
(3) 使酚酞溶液变红。
【设计实验】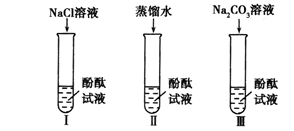
(1)实验Ⅰ的目的是为了验证猜想 不成立。
(2)刘明同学认为实验Ⅱ没必要做,他的理由是 。
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞试液变红。向变红后的溶液中滴加CaCl2溶液至过量,振荡,出现的现象是 ,反应的化学方程式是 。(提示:CaCl2溶液呈中性)
(4)由实验Ⅰ、Ⅱ、Ⅲ得出猜想(3)正确。张宁对此结论有些质疑,于是他查阅资料。
【查阅资料】Na2CO3溶液中,CO2-3和H2O发生如下反应: CO2-3+H2O=====HCO-3+OH-
【得出结论】Na2CO3溶液中使酚酞溶液变红的粒子是 。
某化学兴趣小组根据以下图示进行模拟炼铁的实验,并对产物成分及含量进行探究。
【提出问题】无色气体A有哪些成分?黑色固体B可能是什么?
【查阅资料】(1)常温下,一氧化碳能与氯化钯(PdCl2)溶液反应生成钯(不溶于水)、 二氯化碳和氯化氧。
(2)铁的氧化物都能与稀盐酸、稀硫酸反应,其中氧化铁为红棕色,其余都为黑色,并且只有四氧化三铁能被磁铁吸引。
【提出猜想】猜想1:无色气体A一定是C02,原因是(用化学方程式表示)。
猜想2:黑色固体B全部是铁。
【交流与讨论】小华认为猜想1不一定正确,无色气体中除了CO2外,可能含有CO。
【探究反思】(1)为验证小华的衍箍l,大家按以下图示进行实验,过程与现象如下:
①当X现象为 时,可以确定猜想1是错误的,写出产生该现象的化学方程式: 。
②Ⅱ中无明显现象,但可以往Ⅱ中滴加足量 (填试剂名称或化学式)证明气体在Ⅱ中确实已发生了反应。
(2)为验证猜想2,大家称取7g黑色固体B,按以下图示进行实验探究,过程与现象如下:
①经过分析,大家确定猜想2是错误的,理由是 。
②为了进一步确定黑色固体C的成分,你的方法是 (写出实验操作、现象及结论)。
③实验结束后,称得红色固体的质量为6.4g,则黑色固体B中铁单质的质量分数为 。
化学课外小组设计了一套如图所示的气体发生及收集装置,并探究该装置的多功能性.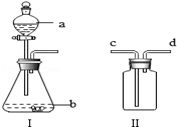
(1)甲同学认为装置Ⅰ可作为实验室制取O2的发生装置,则Ⅰ的a仪器中应加入 ,b仪器中应加入 ,反应的化学方程式为 ,装置Ⅱ中从 管口进气即可作为O2的收集装置.
(2)乙同学认为装置Ⅰ可作为实验室制取二氧化碳的发生装置,则Ⅰ的a仪器应加入 ,b仪器中应加入 .
(3)如果要用装置Ⅱ收集H2,则应从 管口进气.
有一包固体粉末,可能含有氧化钙、氯化钠、碳酸钠、硫酸钠中的一种或几种。为确定其组成,小杨设计出实验方案,实验步骤及现象如下。请回答:
(1)写出步骤④中产生白色沉淀的化学方程式______。
(2)根据实验中的现象,能否确定原固体粉末的组成?若能,请写出各成分的化学式;若不能,在原实验步骤的基础上,对上述方案中的试剂作一改进,并描述相应的实验现象及结论,以确定固体粉末的组成。____________。