实验室常会产生含硫酸的废水,需经处理至中性。某兴趣小组同学配制一定质量分数的氢氧化钾溶液来处理酸性废水。
(l)定性检测废水
检测废水呈酸性的方法是 。
(2)配制200g质量分数为5.6%的氢氧化钾溶液
①计算
m (KOH)= g,V(H 2O)= mL(水的密度近似为1.0g•mL ﹣ 1)。
②称取氢氧化钾
调节托盘天平平衡后,将一只烧杯放在托盘天平的左盘,称量其质量。然后 (按操作先后顺序,填字母),直至天平平衡。
A.向烧杯中加氢氧化钾固体 B.按需要添加砝码、移动游码 C.量取水 D.溶解 E.转移。
(3)定量测定废水
取酸性废水样品100g,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如图所示。(假设废水中其他成分不与氢氧化钾反应且不含硫酸钾)
①P点对应溶液中一定存在的阳离子有 (填离子符号)。
②酸性废水中硫酸的质量分数为 (用百分数表示,保留到0.1%)。
③计算当废水处理至中性时,溶液中硫酸钾的质量分数(写出计算过程,结果用百分数表示,保留到0.l%)。

某化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计实验探究:
[提出问题]甲烷燃烧后生成哪些物质?
[查阅资料]①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;②白色无水CuSO4粉末遇水变蓝色;③CO与人体内的血红蛋白结合,会造成人中毒缺氧。
[猜想与假设]猜想一:CO2、H2O;猜想二:CO、H2O;猜想三:CO2、CO、H2O
[实验探究]将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:

(1)实验过程中观察到A中白色粉末变为蓝色,B、E中澄清石灰水变浑浊,D中红棕色粉末变成黑色,由此推断猜想 成立。
(2)实验过程中B装置的作用是 ;该反应的化学方程式是 。
(3)D装置中发生反应的化学方程式是 。
(4)实验过程中用纯净O2而不用空气的原因是 。
(5)实验过程中B、C装置的顺序不能颠倒,原因是 。
[反思与交流]日常生活中,使用含碳燃料定要注意通风,防止 中毒。
结合下列化学实验装置,回答有关问题。

(1)写出图中标有字母的仪器的名称:a ,b 。
(2)实验室用氯酸钾制取氧气时应选择 (填代号)作为发生装置。常温下,下列收集氧气的方法不可行的是 (填字母序号)。
a.向上排空气法
b.向下排空气法
c.排水法
(3)用装置E收集实验室制取的二氧化碳,气体应从 (填“①”或“②”)端进入。
(4)实验室常用装置C代替装置B制取气体,装置C的优点是 。
实验室有一瓶久置的氢氧化钠固体,经检验只含有NaOH和Na2CO3两种物质。现取该固体样品12.5g溶于水配制成溶液。然后向溶液中滴加稀硫酸,同时收集反应产生的气体。当溶液中的溶质恰好全部转化成Na2SO4时,立即停止滴加稀硫酸。将产生的气体干燥后测定其质量为2.2g(假定溶液中无气体残留)。回答下列有关问题:
(1)写出碳酸钠与硫酸反应的化学方程式: 。
(2)氢氧化钠固体样品中NaOH的质量为 。
(3)计算所加稀硫酸的体积(稀硫酸的溶质质量分数为40%,密度为1.3g/cm3)。
[要求:第(3)小题写出计算过程且计算结果保留到小数点后1位]
浓硫酸与木炭在加热条件下可发生反应产生水和化学式为XO2型的气体。某化学课外兴趣小组的同学对XO2型气体的成分进行了实验探究。
[猜想]
(1)根据反应物组成元素及生成物的化学式类型,提出以下猜想:
|
猜想1 |
猜想2 |
猜想3 |
|
只有CO2 |
只有 SO2 |
CO2和SO2都有 |
[查阅资料]将SO2、CO2气体分别通入下列溶液中产生的有关现象如表:
|
气体 溶液 |
SO2 |
CO2 |
|
品红溶液 |
褪色 |
不褪色 |
|
氯水(黄绿色) |
褪色 |
不褪色 |
|
澄清石灰水 |
浑浊 |
浑浊 |
[实验探究]
实验一:
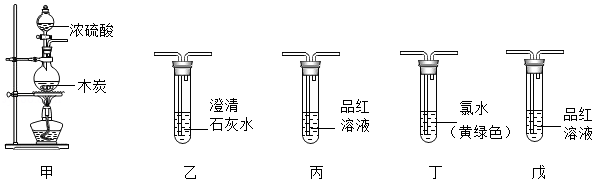
(2)将装置按甲→丙→(尾气处理)连接并进行实验。实验过程中观察到丙中溶液褪色,证明 不成立(填“猜想1”、“猜想2”或“猜想3”)。
实验二:
(3)将装置按甲→乙→(尾气处理)连接并进行实验。实验过程中观察到乙中澄清石灰水变浑浊。根据此现象能否确定CO2 的存在,理由是 。
实验三:
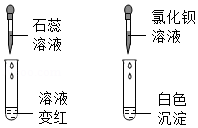
(4)将装置按甲→丙→丁→戊→乙→(尾气处理)连接并进行实验。实验过程中观察到丙、丁中溶液均褪色,戊中溶液颜色无变化,乙中澄清石灰水变浑浊。
①将反应后丁中溶液分成两等份分别置于两支试管中,并按如图所示操作进行实验。根据图中实验现象可判断反应后丁中溶液存在的离子有 。
②丁中溶液的作用是 。
[实验结论]
(5) (填“猜想1”、“猜想2”或“猜想3”)成立。
[问题讨论]
(6)在实验三中,若去掉装置戊,对实验结论 (填“有”或“无”)影响,理由是 。
某实验小组用KClO3和MnO2制取氧气,然后从制取后的残留固体中回收MnO2并用于实验室制取氯气(Cl2 )。部分实验装置如图所示。回答下列问题:

(1)写出装置Ⅰ中制取O2 的化学反应方程式: 。
(2)将制取氧气后的残留固体冷却、转移、 (填操作名称)、过滤、洗涤和干燥,即回收到MnO2.过滤装置Ⅱ中,仪器M的名称是 。
(3)将回收到的MnO2用于实验室制取Cl2.反应原理为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,实验装置为Ⅲ和Ⅳ,实验时,将a口连接 (填“b”或“c”)口收集Cl2,收集到的Cl2中的杂质有 (填化学式)。
MnCl2+Cl2↑+2H2O,实验装置为Ⅲ和Ⅳ,实验时,将a口连接 (填“b”或“c”)口收集Cl2,收集到的Cl2中的杂质有 (填化学式)。
(4)洁厕灵(主要成分为盐酸)与“84”消毒液(主要成分为NaClO)混合也会反应生成Cl2:2HCl+NaClO═R+Cl2↑+H2O,生成物R的化学式为 。