小君和小英同学发现:带火星的竹签在空气中不会复燃,若用装有60%水的集气瓶倒置在水槽中收集氧气,得到的气体能使带火星的竹签复燃。为了找到能使带火星竹签复燃的氧气含量最小值,他们进行了如下探究:
【设计实验】小君设计了如图的装置,该装置的圆底烧瓶中放入25毫升水的目的是 。
【实验研究】第一组实验:取3只集气瓶,编号为①②③,分别装入15%、30%和45%的水,盖上盖玻片倒置在水槽中。当气泡 放出后,导管口伸入集气瓶把其中的水全部排出,将相同的3支带火星竹签分别插入①~③号瓶中,记录实验现象。
获得第一组实验现象后,小君又做了第二组实验,并记录实验现象。两组实验数据和现象见下表:
实验分组 |
第一组 |
第二组 |
||||
实验序号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
集气瓶装水的体积分数/% |
15 |
30 |
45 |
34 |
38 |
42 |
带火星竹签状况 |
亮 |
很亮 |
复燃 |
很亮 |
复燃 |
复燃 |
得出上述两组实验现象后,小英认为还不能确定能使带火星竹签复燃的氧气含量最小值,需继续进行实验,则实验序号⑦的集气瓶装水的体积分数应该是 %。
【实验结论】再经过数次实验并计算后得出:能使带火星竹签复燃的氧气含量最小值为48.7%。
【继续探究】小君认为采用该方法收集的氧气中含有一定量的水蒸气,请你提出实验改进的措施 。

请根据如图所示回答相关问题。

(1)实验一点燃氢气前要 。
(2)实验二探究的是 对溶解速率的影响。
(3)实验三中,将胶头滴管中的水滴入锥形瓶后,预期观察到的现象是 。
(4)实验四存在的明显错误是 。
气体的制取和性质是初中化学知识的核心之一。结合下列实验装置图回答问题:
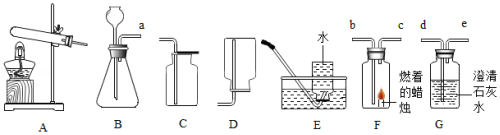
(1)实验室制取二氧化碳的化学方程式为 ,使用B装置制取气体的优点是 。
(2)桢桢同学连接装置B、F、G进行实验。若往B装置中分别加入二氧化锰固体和过氧化氢溶液,且在装置F和G中看到明显的现象,则按气体流向,导管口的连接顺序为a→ (填导管口字母),装置F和G中分别观察到的现象是 。
(3)某气体只能用E装置收集,则该气体可能具有的性质为 (填字母序号)。
a.能与水反应
b.能与空气中某种物质反应
c.密度与空气的密度非常接近
观察实验现象,得出实验结论。
(1)如图所示为实验室用过氧化氢溶液和二氧化锰的混合物制取氧气。写出:

①仪器a的名称 。
②用向上排空气法收集氧气的理由是 。
③该反应的化学方程式为 。
④检验氧气是否集满的方法是 。
⑤红磷在空气中燃烧的现象是 ,发生反应的化学方程式为 。
(2)如图描述的是:酸溶液使指示剂变色的实验,发现紫色石蕊溶液均变为红色,产生这一现象的根本原因是这两种酸溶液都含有 。

(3)在探究影响溶质溶解快慢的因素,比较等量硫酸铜在水中溶解的快慢时,设计并进行了如下实验:
|
实验 |
实验1 |
实验2 |
实验3 |
|
完全溶解所需时间/s |
60 |
35 |
55 |
请你回答下列问题:
①对比实验1和实验2的现象,可以得出的结论是 。
②设计实验2和实验3进行对比实验的目的是 。
(4)化学课上,教师按图甲所示的装置进行实验,得到图乙所示的现象。用初中阶段所学化学知识不能解释的现象是 ,由此可见,人们对事物的认识是一个不断完善和提高的过程。

实验室制取气体时需要的一些装置如图所示,请回答下列问题:

(1)写出标有序号的仪器名称:② ;
(2)写出用A装置制取氧气的化学方程式 ;
(3)实验室制取CO2时,收集装置通常只选择E的原因是 ,若要收集一瓶干燥的二氧化碳,应在E之前连接装置 (填字母);
(4)实验室常用高锰酸钾固体和浓盐酸在常温下应制取氯气(Cl2),用该方法制取氯气时选用的发生装置是 (填字母);如果用G装置收集氯气,气体应从 (填“a”或“b”)口进;氯气有毒,可与水反应生成酸,为防止其污染空气,应选择 性溶液吸收尾气。
如图为初中化学中关于酸、碱、盐化学性质的知识框架图,X、Y是除酸、碱、盐之外的不同类别的物质,据图回答问题:
(1)X的物质类别是 ;
(2)若“盐1”为AgNO3,则反应③的化学方程式为 (任写一个);
(3)反应④能够发生应该满足的条件是 ;
(4)在反应①②③④中,属于中和反应的是 。
