利用如图所示的实验装置制备常见气体,请回答有关问题:

(1)写出标有序号的仪器名称:① 。
(2)装置A为气体发生装置,在试管内的适当位置放入 、 等实验用品以制取氧气,写出有关反应的化学方程式 。
(3)若用装置B收集的氧气不纯,原因可能是 (写一种)。
(4)用装置C收集氧气,验满时将带火星的木条放在 (选填"a"或"b")处。
(5)装置D是用软塑料管自制的气体发生装置,利用该装置制取二氧化碳气体时,塑料管中加入的液体药品是 ,药品加入完毕后,接下来的操作是: 。
请结合图示实验装置,回答下列问题。

(1)实验室用高锰酸钾制取氧气的化学方程式为 ,A装置试管口塞一团棉花的原因是 。收集氧气可以选用 (从C、D、E装置中选择)装置。
(2)实验室使用B装置制取二氧化碳的突出优点是 。将制得的二氧化碳通入紫色石蕊溶液中,观察到的现象是 。
(3)某氢气中混有少量的水蒸气,欲使用F、G装置除去少量的水蒸气并收集氢气,则装置的连接顺序为 (用端口字母表示)。
下列是初中化学常见仪器与实验。
(1)A图中仪器的名称是 。
(2)取用块状大理石用到的是 (填字母)图中仪器。
(3)D图为检验氧气是否收集满的操作,请将明显的错误加以改正 。
(4)E图中能够说明Cu和Ag活动性顺序的现象是 。
元旦晚会上,物质王国中常见的六种物质甲、乙、丙、丁、戊、己跳起了欢快
的“锅庄舞”。已知丁物质常用作食品干燥剂,己物质是炉具清洁剂中含有的物质。它们的位置关系如图所示,“一”表示物质之间可以反应,“→”表示物质之间可以转化(部分反应物、生成物及反应条件已略去)。回答下列问题:
(1)乙物质的化学式为 。
(2)写出图中序号所对应反应的化学方程式:
① ;
② 。
(3)不慎将己物质的浓溶液沾到皮肤上,应先用大量的水冲洗,再涂上 (填名称)溶液。
(4)上述反应及转化关系中共涉及 种基本反应类型。
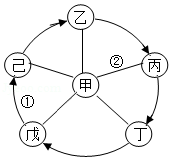
已知某水泥样品的主要成分是氧化钙、二氧化硅,并含有一定量的氧化铝、氧化镁等金属氧化物。国家标准实验中测定水泥中钙含量的方法之一是通过高锰酸钾对CaC2O4进行滴定。其流程如图:
已知:①二氧化硅既不溶于水也不与酸反应。
②氨水显碱性,化学性质与氢氧化钠相似。
(1)pH=5.5的溶液显 (填“酸”、“碱”或“中”)性。
(2)水泥样品中加入盐酸的目的是 。
(3)步骤Ⅰ与步骤Ⅱ中涉及的操作名称是 ,固体A的化学式为 ,固体B中含有物质的化学式为 (任写一个)。
(4)步骤Ⅲ中生成CaC2O4的化学方程式为 。
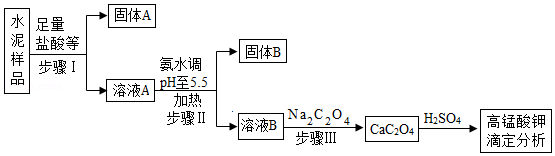
类价二维图反映的是元素的化合价与物质类别之间的关系,构建类价二维图是化学学习的重要方法。图1是某同学绘制的关于碳元素的类价二维图。
(1)a处氢化物为天然气的主要成分,其化学式为 :b处对应物质的类别是 。
(2)煤的主要成分是单质碳。图2是用煤合成水煤气的反应微观示意图。
该反应中方框丁中微粒的图示为 ,甲对应的物质表现出了 性。
(3)类价二维图中的物质在一定条件下可以相互转化。请从含碳物质中选择合适物质完成下列表格:
|
转化类型 |
转化的化学方程式 |
反应用途 |
|
碳元素化合价升高 |
|
工业炼铁 |
|
碳元素化合价不变 |
NaHCO3+HCl=NaCl+CO2↑+H2O |
|