金属钴(Co)在国防工业中有重要应用。某矿石中含钴的氧化物(CoO、Co2O3)研究人员在实验室用硫酸酸浸的方法提取钴元素,并探究最佳提取条件
(1)写出下列化合物中Co元素的化合价:CoO ,Co2O3 。
(2)酸浸时钴的氧化物发生如下反应:
反应I CoO+H2SO4═CoSO4+H2O
反应Ⅱ2Co2O3+4H2SO4═4CoSO4+O2↑+4H2O
反应ⅢCo2O3+2H2SO4+Na2SO3═2CoSO4+2H2O+Na2SO4
①反应后溶液中含钴元素的微粒是 (填化学符号)
②已知反应前矿石中CoO的质量为ag,Co2O3的质量为bg,则理论上可以生成CoSO4 g(用含a、b的式子表示)
(3)为探究最佳提取条件,将矿石在一定条件下酸浸4小时,测量钴元素的浸出率部分数据如下:
编号 |
矿石用量(g) |
硫酸用量(g) |
Na2SO3用量(g) |
温度(℃) |
钴元素浸出率(%) |
1 |
85.71 |
12.62 |
0 |
85 |
56.39 |
2 |
85.71 |
6.31 |
0 |
85 |
49.98 |
3 |
85.71 |
6.31 |
0 |
65 |
43.33 |
4 |
85.71 |
6.31 |
0.43 |
65 |
73.95 |
5 |
85.71 |
6.31 |
0.86 |
65 |
74.77 |
①本实验研究了哪些因素对钴元素浸出率的影响 ;
②根据上表数据,其他条件不变,温度升高,钴元素的浸出率 ;
③工业生产中采用实验 (填编号)的提取条件更合理。
人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1) 现代社会使用大量的钢铁,钢铁与接触容易生锈造成损失,在钢铁表面采用方法可以防止钢铁生锈。
(2) 波尔多液是由硫酸铜和熟石灰加水配制而成,不能用铁制容器配制的原因是(用化学方程式表示) 。
根据下表信息,完成表中空格:
| 化学符号 |
2H2 |
Mg2+ |
||
| 符号的意义 |
2个氮原子 |
五氧化二磷中磷元素的化合价为+5价 |
长时间腌制的蔬菜中含有致癌物亚硝酸钠(NaNO2),它是硝酸钠(NaNO3)在一定的条件下反应生成的,现有一包含有硝酸钠的亚硝酸钠样品,测得其中的含氮量为28%,那么含氧量为。
元素周期表是学习化学的重要工具。下面是元素周期表中1~18号元素原子核外电子排布,我们对它进行研究: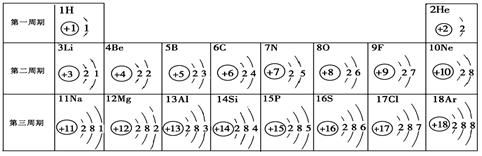
⑴ 第16号元素属于_______元素(填“金属”或“非金属”),它在化学反应中容易________(填“得”或“失”)电子;
⑵ 元素的化学性质与原子结构中的______________数关系密切;
⑶ 在同一族中,各元素的原子结构呈现的规律有________________(任写一点);
⑷ 研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
奇妙的化学王国里,没有生命的阿拉伯数字也变得鲜活起来。这些数字在化学符号周围不同的位置上,将代表着不同的含义。例如:2N SO2 Zn2+等。请你试着再写出两个带有数字“2”但含义不同的化学符号:①_________________________;②__________________________。
SO2 Zn2+等。请你试着再写出两个带有数字“2”但含义不同的化学符号:①_________________________;②__________________________。
(2)在一个陌生的星球上充满了一种浅黄绿色的气态单质。科学家研究了该单质,确定其化学式为F2,进一步研究表明:当该元素原子与金属元素原子化合时,只能形成F-。试回答:
①根据上面提供的信息判断,F元素属于____________(填“金属”或“非金属”)
②科学家在该星球上还发现了另一种元素,确定其元素符号为Al,当Al原子与F原子化合时Al显+3价,则这种化合物的化学式为_______________