某校进行九年级化学实验技能考查,确定了以下三个考题:①粗盐提纯;②实验室制取和收集二氧化碳;③实验室制取和收集氧气.考查规定由学生抽签确定考题.
甲同学抽签后被监考老师引导至准备了下列仪器和药品的实验台前:
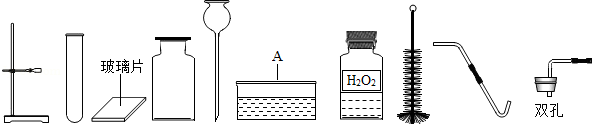
(1)如图中仪器A的名称是 ;分析抽签确定的考题,甲同学发现其中缺少了一种药品,向老师申请补充后完成实验.请写出该实验的化学反应方程式 .
(2)以下是甲同学实验时的主要步骤,这些步骤的正确顺序是 (填字母标号).
A.制备气体 B.收集气体
C.检查装置的气密性 D.清洗仪器,整理试验台
若另选药品,也能完成另一个考题,发生的化学反应方程式为 .
某化学兴趣小组利用所学知识制取氢氧化钠溶液。他们向盛有一定量碳酸钠溶液的烧杯中加入一定量的澄清石灰水,充分反应后过滤。甲同学认为滤液就是氢氧化钠溶液,其余同学不同意他的说法,大家一起展开探究。
[提出问题]滤液中的溶质成分是什么?
[猜想假设]猜想一:氢氧化钠
猜想二:氢氧化钠、氢氧化钙
猜想三:氢氧化钠、碳酸钠
猜想四:氢氧化钠、氢氧化钙、碳酸钠
[讨论交流]大家一致认为猜想四不成立,请用化学方程式说明理由: 。
[实验探究]甲、乙、丙三位同学分别取少量滤液于试管中,进行了下列实验。
|
实验操作 |
现象 |
结论 |
|
|
甲同学 |
加入足量 稀盐酸 |
无明显现象 |
猜想一 成立 |
|
乙同学 |
加入碳酸 钠溶液 |
无明显现象 |
猜想一 成立 |
|
丙同学 |
加入无色 酚酞溶液 |
溶液变为红色 |
猜想一 成立 |
[实验评价]甲同学的实验只能证明滤液中不含 ;乙同学的实验只能证明猜想二不成立;丙同学的实验错误,原因是 。
[得出结论]综合 两位同学的实验和现象,可证明猜想一成立。
[反思迁移]①同学们经过讨论,提出用两种盐溶液及相应的实验操作,也可确定所得滤液中溶质的成分,这两种盐溶液可以是 。
②在制取某物质时,除了根据反应原理设计实验,还需要注意 。
现有以下实验仪器和火柴、棉花、玻璃片等必要的实验用品,回答下列问题。

(1)若用高锰酸钾制取氧气,还需补充的仪器名称是 。
(2)实验室若要制取二氧化碳气体,从仪器G中加入的药品名称是 。
(3)若用二氧化锰和过氧化氢溶液制取并收集较多量氧气,应选择的仪器组合是 (填字母),反应的化学方程式是 。
某学校组织社会调查,同学们考察了一家化工企业的污水处理情况。企业技术人员用氢氧化钙粉末对中和池内的296kg污水进行中和处理(污水中的主要污染物是盐酸),测定处理后水样的pH等于7,请回答:
(1)技术人员称量9.0g氢氧化钙粉末,示意图如图所示。请你写出所选砝码的质量 和游码的示数 。
(2)假设上述氢氧化钙与中和池内污水中的盐酸恰好完全反应(污水中的其他成分均不与氢氧化钙反应),计算污水中HCl的质量分数是多少?(写出计算过程)
小明在老师的指导下和同学们一起对实验室中一瓶久置的过氧化氢溶液进行了如下探究,请你参与他们的探究活动。
实验I 在试管中加入5mL过氧化氢溶液,将带火星的木条伸入试管口,木条未复燃。
实验II 给上述试管加热,有气泡产生,将带火星的木条伸入试管口,木条仍未复燃。
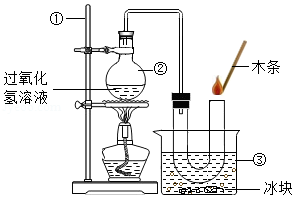
实验III 用如图装置进行实验,带火星的木条复燃。
请回答下列问题:
(1)写出编号仪器的名称:① ,③ 。
(2)如图所示,安装好实验装置后,首先进行的操作是 ,写出②中发生的化学方程式 ,冰水的作用是 。
(3)小明另取一支试管,向其中加入5mL过氧化氢溶液并加入少量二氧化锰,将带火星的木条伸入试管口,木条复燃,二氧化锰的作用是 。通过以上探究活动得知,预使物质燃烧,除达到可燃物的着火点外,还应满足的条件是 。
下列是实验室制取气体常用的部分装置。
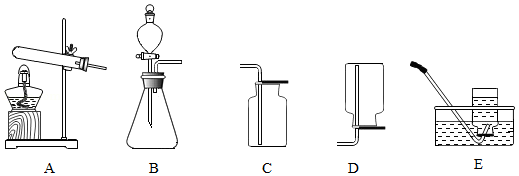
(1)同学们为了探究影响实验室制取二氧化碳气体的因素,进行了以下四组实验:
|
药品/实验编号 |
甲 |
乙 |
丙 |
丁 |
|
大理石 |
mg,块状 |
mg,块状 |
mg,粉末状 |
mg,粉末状 |
|
盐酸(过量) |
vmL,稀盐酸 |
vmL,浓盐酸 |
vmL,稀盐酸 |
vmL,浓盐酸 |
①写出上述反应的化学方程式 ,此反应属于的基本反应类型是 ,
原来收集二氧化碳气体的装置是 (填写字母)。
②若探究盐酸的浓度对上述反应的影响,可选择实验甲与 (选填实验编号)进行对照。
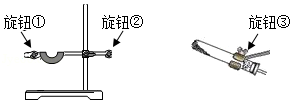
(2)小丽同学选用A装置加热高锰酸钾制取氧气时发现试管固定的太高,应调节图中的旋钮 (选填“①”、“②”、“③”)。
(3)通过比较,归纳实验室制取二氧化碳和氧气的实验,总结实验室制取气体选择装置时的一般思路。
|
选择气体发生装置的依据 |
|
|
选择气体收集装置的依据 |