已知:①NaHCO3 固体受热分解 2NaHCO3 Na2CO3+CO2↑+H2O;②Na2CO3 受热不分解。回答下列问题:
(1)关于 NaHCO3 固体的叙述错误的是 (填标号)。
A.俗称小苏打 B.难溶于水
C.可与稀盐酸发生反应 D.是发酵粉的主要成分之一
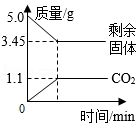
(2)欲测定某 NaHCO3固体样品(只含Na2CO3杂质且分布均匀)中NaHCO3的质量分数,将 5.0g 该样品加热至质量不再改变,测得剩余固体的质量、生成CO2的质量随时间变化如图所示。
①NaOH溶液的pH 7(填“>”、“=”或“<”),用该溶液将生成的CO2完全吸收,发生反应的化学方程式为 。
②由图中数据可知,上述5.0g NaHCO3 样品完全分解产生CO2的质量为 g,产生H2O的质量是 g。
③计算该样品中NaHCO3的质量分数(根据化学方程式写出完整的计算步骤)。
已知KNO3在20℃时的溶解度是31.6g,求此温度下将15.8g KNO3固体溶于水配成饱和溶液,需加水 克,所得溶液的溶质质量分数是 。
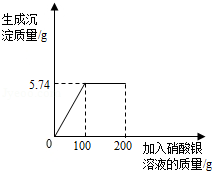
将含有可溶性杂质的某氯化镁样品3g溶于足量水中得到不饱和溶液,再向所得溶液中逐滴滴入200g一定溶质质量分数的AgNO3溶液(杂质不含镁元素且不与AgNO3溶液反应)。实验过程中,生成沉淀的质量与滴入AgNO3溶液的质量关系如图所示:
试计算:
(1)恰好完全反应时生成沉淀质量为 g。
(2)样品中含镁元素的质量是多少?(结果精确到0.01g)
(3)原硝酸银溶液中溶质的质量分数是多少?(结果精确到0.1%)
氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得知:氢化钙(CaH2)遇水反应生成氢氧化钙和氢气。探究斯小组的同学把一定量的CaH2 加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
[提出问题]滤液中溶质的成分是什么?
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因 。
[实验验证]
|
实验 |
现象 |
结论 |
|
(1)取少量滤液,向其中滴入少量碳酸钠溶液 |
无明显现象 |
猜想 不成立 |
|
(2)另取少量滤液,向其中加入足量稀盐酸 |
|
猜想三成立 |
[反思与拓展]
(1)写出氢化钙(CaH2)与水反应的化学方程式 。
(2)若向NH4Cl的溶液中加入一定量的CaH2,充分反应,产生的气体有氢气和 。
(3)登山运动员携带CaH2作为能源提供剂与携带氢气相比,其优点是 (写一条即可)。
实验室部分仪器或装置如图所示,请回答下列问题。
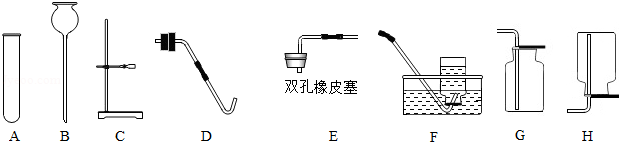
(1)若要组装一套实验室制取二氧化碳的发生和收集装置,可选择图中 (填仪器或装置的标号),实验室用该装置制取二氧化碳的化学方程式为 。
(2)若用高锰酸钾制取氧气,你认为还需要增加的玻璃仪器是 ;写出该反应的化学方程式: 。
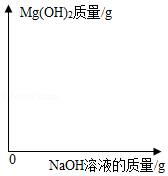
Mg(OH)2具有广泛的应用,常用菱镁矿制备。研究人员向一定质量的菱镁矿粉中加入过量的稀硫酸,充分溶解后除杂、过滤,得到只含MgSO4和H2SO4的混合溶液,为确定混合溶液中镁的含量,取4份混合溶液各100g,向每份混合溶液中加入一定质量的4%NaOH溶液,得到实验数据如下表所示:
|
实验编号 |
① |
② |
③ |
④ |
|
NaOH溶液质量/g |
10.0 |
20.0 |
30.0 |
40.0 |
|
Mg(OH)2质量/g |
0.232 |
0.522 |
0.580 |
0.580 |
(1)实验 (填实验编号)中硫酸镁完全反应。
(2)计算100g混合溶液中含MgSO4的质量(写出计算过程)。
(3)分析实验数据,在图中,画出加入4% NaOH溶液质量0﹣30.0g过程中,产生Mg(OH)2沉淀质量对应的变化图,并标注必要的数值。