我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作还原剂把氧化铜中的铜还原出来,小明查阅了大量的资料后,建议用超细炭粉与氧化铜粉末混合进行实验,他的理由是 .
(1)同学们按如图装置进行实验,当看到澄清的石灰水刚刚出现浑浊时, (填写"可以"或者"不能")确定氧化铜和炭粉已经开始反应.
(2)为了使氧化铜中的铜完全被还原,对于下列三组氧化铜和炭粉的质量比例,你建议选择 (填写字母),简要说明你的理由 .
A.36:3 B.40:3 C.48:3.
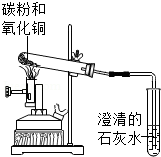
A~E为初中化学常见物质,他们之间有如图所示的转化和反应关系 (“→”表示某一种物质经一步反应可转化为另一种物质,“一”表示相连两种物质能发生化学反应,部分反应物、生成物及反应条件已略去)。
(1)若C、D是组成元素相同的气体,且A和X反应的现象是固体由红色逐渐变成黑色,则A为 ,B为 ,D与E发生的化学反应 (填“是”或“不是”)置换反应。
(2)若A、B、C、D、E均含有一种相同的元素,且A、B、C、D是不同类别的物质,A和X反应的现象是有刺激性气味的气体生成,则D为 ,写出A﹣B反应的化学方程式 。

(1)早在春秋战国时期,我国就开始生产和使用铁器.用铁锅炒菜主要是利用铁具有良好的 性,铁锅存放不当容易生锈,铁生锈的条件是 .
(2)实验室采用还原法制备新型材料纳米级铁粉,其流程如图所示:

①纳米级铁粉在空气中易燃烧,其生成物的名称为 .
②实验中通入N2的目的是 .
③Ⅱ中反应的化学方程式为 .
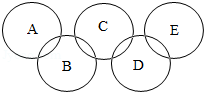
第31届夏季奥林匹克奥运会于今年8月5日至21日在巴西举行,奥运五环旗将在南美洲上空飘扬,现有A﹣E分别为盐酸、硫酸钠溶液、碳酸钠溶液、氯化钡溶液、氧化铜的五种常见物质,存在类似“奥运五环”的如图图示反应关系.已知常温下相连环的物质间能发生反应,不相连环的物质间不能发生反应,其中B常用于除铁锈.
请回答下列问题:
(1)写出化学式:A ,D .
(2)A+B反应的化学方程式为 .
(3)C+D反应的化学方程式为 .
铝、铁、铜是人类广泛使用的三种金属,与我们的生活息息相关,
(1)用铜块制成铜片、铜丝利用了铜的 性。钢铁制品容易发生锈蚀,在其表面涂油漆的防锈原理是 。
(2)把两块大小相同且洁净的铁片、铜片分别投入浓度相同的稀硫酸中,请描述你观察到的现象并分析其中的原因。
(3)将纯铝和铝合金相互刻划,纯铝上留下明显划痕。请你解释其中的原因。
(4)自行车用到大量铝合金材料,外形美观,材质轻硬、牢固,除了代步,还可以作为健身工具。由此你对化学与人类生活的关系有何感想(任写一点)?
结合下列实验装置,回答:
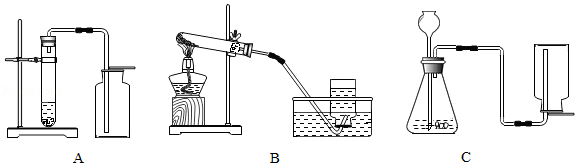
(1)实验室若用分解暗紫色固体制取O2,该固体的名称是 ,可选 (填字母,下同)装置。若用分解H2O2溶液制取O2,可选 装置。
(2)探究CO2性质的装置Ⅰ、Ⅱ如下:

①装装置Ⅰ,将Y形导管平放于桌面上,通入CO2后,观察到a管中试纸变红色,
b管中试纸无明显变化,此现象说明CO2能与 反应,生成的 使紫色石蕊变红色。
②装置Ⅱ,将Y形导管固定在铁架台上,a管在上方,b管在下方,通入CO2后,观察到b管中试纸先变红色且颜色较深,a管中试纸后变红色且颜色较浅,此现象说明CO2具有①所验证的性质外,还说明CO2的 。
(3)实验室制取CO2的化学方程式为 ,应选 (填字母)装置,选择该装置的理由是 。