工业上常用电解饱和食盐水的方法制取烧碱,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
(1)取少量样品于烧杯中,向其中加入过量稀盐酸,观察到有气泡产生,说明样品中含有 ,该反应的化学方程式为 ,接着又向烧杯中继续加入硝酸银溶液,出现了白色沉淀,甲同学立刻得出结论:样品中还含有氯化钠,乙同学对该结论提出了质疑,认为不一定含有氯化钠,理由是 ;
(2)丙同学认为除了需要确认是否含有氯化钠外,还需要确认样品中是否含有氢氧化钠,于是,大家又进行了以下实验:
①另取少量样品溶解于水,向其中加入过量硝酸钙溶液,产生白色沉淀,然后过滤、洗涤;
②向滤液中加入足量稀硝酸,再滴入硝酸银溶液后产生白色沉淀;
③向滤渣中加少量水后滴入酚酞,溶液变红.
由此判断,滤渣中的物质是 (填化学式).
(3)根据以上经验,得出的结论正确的是 (填序号)
| A. |
样品中无NaCl |
| B. |
样品中只有NaOH和Na 2CO 3 |
| C. |
样品中无NaOH |
| D. |
样品中有Na 2CO 3、NaOH和NaCl. |
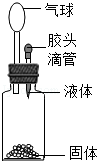
如图,用胶头滴管向装有固体的广口瓶中滴加液体,能使气球变大,则使用的固体和液体可能是:(请写出三种组合)
(1) ;
(2) ;
(3) 。
亚硝酸钠是一种工业用盐,它有毒、有咸味,外形与食盐相似。人若误食会引起中毒,危害人体健康,甚至致人死亡。亚硝酸钠的水溶液呈碱性,食盐水溶液呈中性。请你根据所学的知识,设计实验来鉴别亚硝酸钠和食盐并填写下表:
|
实验步骤 |
实验现象 |
实验结论 |
将8.0g三氧化二铁加入到100.0g的稀硫酸溶液中,恰好完全反应。化学反应方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.试计算:
(1)硫酸的相对分子质量是 ;
(2)稀硫酸溶液的溶质质量分数(计算结果精确到0.1%)。
粮食、蔬菜、肉类、豆制品等食物是我们日常营养的主要来源。菠菜营养丰富,豆腐中含有丰富的蛋白质及钙盐等,但民间有“菠菜、豆腐不宜同食”的说法。某化学兴趣小组针对此说法进行探究。
[查阅资料]①菠菜含有丰富的铁、草酸盐、碳酸盐等;②草酸钙(CaC2O4)不溶于水,不易被人体吸收;③醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐等。
[提出猜想]“菠菜、豆腐不宜同食”的原因可能是 。
[实验探究]

(1)加入足量CaCl2溶液的目的是 。
(2)已知气体C能使澄清石灰水变浑浊,写出该反应的化学方程式 。
(3)醋酸的化学式可简写为HAc.写出步骤④发生的化学反应方程式 。
(4)白色沉淀B的主要成分是 (填化学式)。可见菠菜中的草酸盐能与钙盐反应生成草酸钙。
[反思与应用]家庭中常常将菠菜放在开水中烫过后再烹饪,其目的是 。
气体的实验室制取是学生必备的基本实验技能,请根据下列装置回答问题:

(1)写出图中标数字的仪器名称① ② 。
(2)实验室用加热高锰酸钾制取氧气的化学反应方程式为 ,若用D装置收集氧气,气体应从管口 (填“a”或“b”)进入。用E装置进行氧气性质实验时,E装置中水的作用是 。
(3)装置中既能制O2又能制CO2的发生装置是 (填字母序号),用C装置收集CO2的原因是 。
(4)图中的F装置可用来测量生成氧气的体积。进行操作时,集气瓶未装满水是否影响实验结果 (填“是”或“否”)。