娄底人在端午节有吃皮蛋的习俗。某化学小组的同学查阅资料后得知,腌制皮蛋的主要原料有:生石灰、纯碱和食盐。同学们向这三种物质中加入适量水,充分搅拌,过滤,对滤渣中溶质的成分进行探究。
小组同学讨论后一致认为,滤液中的溶质一定含有NaCl和 。(写化学式)
【提出问题】滤液中还可能含有哪些溶质呢?
【作出猜想】
2
23
223
【交流讨论】经过进一步讨论,大家认为小华的猜想不合理,原因是: 。(用化学方程式表示)
【实验探究】
实验操作 |
实验现象 |
实验结论 |
小林:取少量滤液于试管中,滴加足量的稀盐酸 |
|
小方的猜想正确 |
小方:取少量滤液于试管中,滴加 溶液 |
产生白色沉淀 |
小方的猜想正确 |
23溶液 |
无明显现象 |
小方的猜想正确 |
【交流谈论】同学们认为,通过小华的实验不足以得出其结论,原因是 。
【继续探究】小明也取少量滤液于试管中,滴加稀盐酸,却没有看到明显现象,小明对此深感疑惑。
【解释评价】经老师的指导和大家的认真思考后终于找出了原因,你认为是 。最后,老师对同学们这种严谨的科学态度给予了充分的肯定。
某化学兴趣小组同学为回收一块质量为40g的铜锌合金中的铜,将该合金放入烧杯中,逐渐加入稀硫酸至不再产生气泡时,恰好用去稀硫酸100g,烧杯内剩余固体27g。
请完成下列分析及计算。
(1)40g铜锌合金中锌的质量是 g。
(2)计算所用稀硫酸中溶质的质量分数。
乙基麦芽酚(C7H8Ox)是一种安全无毒的理想食品添加剂,是烟草、食品、饮料、香精等良好的香味增效剂,对食品的香味改善具有显著效果,且能延长食品储存期。请计算:
(1)乙基麦芽酚的相对分子质量为140,则x的数值为 。
(2)乙基麦芽酚中碳、氢、氧三种元素的质量比为 。
实验室有一包白色粉末,可能由Na2SO4、Na2CO3、CuSO4、NaOH,BaCl2中的一种或几种组成。为探究其组成设计并进行了以下实验:
步骤一:取少量白色粉末于烧杯中,加入足量的水溶解,并用玻璃棒充分溶解,搅拌、过滤,得到无色滤液和白色沉淀。
步骤二:取少量无色滤液于试管中,向其中加入 ,溶液变红。
步骤三:向白色沉淀中加入足量的稀盐酸沉淀全部溶解。
请分析上述实验现象,回答下列问题
(1)白色粉末中一定不含 ,可能含有 。
(2)请写出生成白色沉淀的化学方程式 。
[提出问题]溶液中显碱性的物质是什么?
[作出猜想]猜想I:Na2CO3 猜想Ⅱ:NaOH 猜想Ⅲ: 。
[查阅资料]同学们查阅资料得知NaCl、BaCl2溶液呈中性
[进行实验]
取步骤一中的无色滤液于试管中滴加过量的BaCl2溶液观察到 的现象,说明白色粉末中含有碳酸钠;静置后,再向该试管中滴加酚酞溶液,溶液变红,说明白色粉末中还含有 。
[得出结论](3)该白色粉末的成分是 。
通过一年的化学学习,相信你已经初步掌握了实验室制取气体的有关知识。结合图示回答问题。
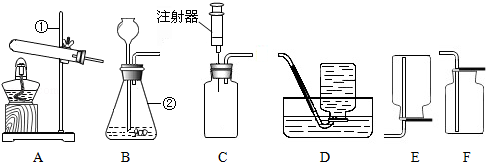
(1)写出图中标示的仪器名称:① ,② 。
(2)甲同学用高锰酸钾制取氧气时应选择的发生装置是 (填代号),用该方法制取氧气的化学方程式为 ;用排水法收集氧气,实验结束后,他发现水槽中的水变红了,请你帮她分析可能的原因: 。
(3)乙同学在实验室想制取CO 2气体,她应选用的药品是 ,可用 (填代号)装置收集CO 2。
(4)装置B和装置C都可以用于制取同种气体,装置C的优点是 。
学会使用常见的化学实验仪器,并能规范地进行实验操作,是学习化学的基本要求。如图是化学实验室中常用的几种仪器和一个常见的实验。请回答下列问题。

(1)图一中能直接加热的玻璃仪器是 (填代号);仪器a的用途是 。
(2)王潇同学欲用图一所示的仪器做硫在氧气中燃烧的实验,他应选用的仪器是 。
(3)指出如图二所示实验操作的错误之处 。