现有一家庭使用纯碱样品,其中含杂质氯化钠(不含其它杂质),为了测定样品中杂质氯化钠的质量分数,李明同学进行了三次实验。实验数据如表。
编号 |
第1次 |
第2次 |
第3次 |
所取固体样品的质量/g |
15 |
12 |
12 |
加入氯化钙溶液的质量/g |
100 |
100 |
150 |
反应后生成沉淀的质量/g |
10 |
10 |
10 |
完成下列计算(计算结果精确到0.1%):
(1)样品中氯化钠的质量分数;
(2)加入氯化钙溶液的溶质质量分数;
(3)恰好完全反应时,反应后所得溶液中氯化钠的质量分数。
实验室现有稀硫酸、稀盐酸、石灰石、锌片等药品及相关仪器,请结合如图的装置回答问题:
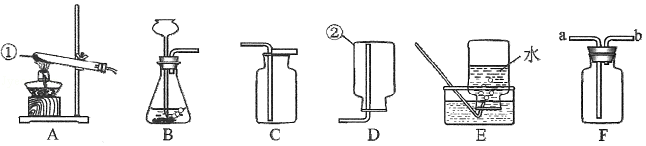
(1)写出如图中标有序号的仪器名称:① ;② 。
(2)欲用装置F收集氢气,应该从装置F的 (填“a”或“b”) 端通入气体。
(3)某气体只能用E装置收集,则该气体不能具有的性质是 (填序号)。
A.易溶于水或与水反应
B.能与空气反应
C.密度与空气接近
(4)若用如图中的装置制取二氧化碳,选择的装置组合是 (填字母),该反应的化学方程式是 。
城市的生活用水是经自来水厂净化处理过的。如图是自来水厂净化水的过程示意图。

(1)在自来水厂净化自来水的过程中,a池的作用主要是 (填序号)。
A.沉淀
B.过滤
C.吸附
D.蒸馏
(2)取水后加入絮凝剂(明矾)的作用是 。
(3)在处理过的水样中加入一定量的肥皂水并振荡,观察到泡沫较少,浮渣较多。说明该水样属于 (填“硬水”或“软水”)。
(4)在投药消毒步骤中所发生的变化是 (填“物理变化”或“化学变化”)。
(5)水资源短缺会影响人民生活,制约经济发展。请举出一种节水的措施 。
某工厂利用废硫酸溶液与铁反应制取硫酸亚铁。49t废硫酸溶液中的硫酸与5.6t铁恰好完全反应。求:
(1)废硫酸溶液中溶质的质量分数。
(2)理论上生产的硫酸亚铁的质量。[温馨提示:Fe+H2SO4═FeSO4+H2↑]
某教师在进行“常见的碱”的教学时做了以下演示实验:取少量纯净的氢氧化钠固体于50mL干燥的烧杯中,置于电子天平上。一段时间后,氢氧化钠固体表面出现了液体,天平示数增加。取下烧杯,将其放置在空气中。一周后,向烧杯中加适量水配制成溶液,取少量烧杯中的溶液于试管中,滴加足量稀盐酸,观察到有气泡冒出。
[交流与解释]
(1)氢氧化钠固体表面出现液体是因为氢氧化钠吸收空气中的水分而潮解。
(2)电子天平示数增加的原因除了吸收水分以外,还有另一个原因是 (用化学方程式表示)。
教师安排兴趣小组同学对烧杯中的溶液是否还含有氢氧化钠进行了以下探究。
[作出猜想]猜想一:有氢氧化钠
猜想二:没有氢氧化钠
[查阅资料]BaCl2溶液、NaNO3溶液、Ba(NO3)2溶液均呈中性。
[进行实验]小明同学取少量烧杯中的溶液于试管中,滴入几滴无色酚酞,观察到溶液变红,小明同学认为猜想一成立。
[交流与评价]小玲同学认为小明同学的结论不一定正确,原因是 。于是,小玲同学继续进行探究。
[进行实验]
|
实验操作 |
实验现象 |
实验结论 |
|
小玲同学在小明同学所做实验后的溶液中,滴入足量的Ba(NO3)2溶液, |
|
猜想一成立 |
[反思与拓展]
(1)根据氢氧化钠固体易潮解的性质,可用氢氧化钠固体作某些气体的 。
(2)另取少量烧杯中的溶液进行以下实验,也能证明猜想一成立的是 (填序号)。
A.先加足量稀盐酸,再滴加紫色石蕊溶液
B.先加足量BaCl2溶液,静置,取上层清液,再滴加CuCl2溶液
C.先加足量Ca(OH)2溶液,静置,取上层清液,再滴加酚酞溶液
D.先加足量Ba(NO3)2溶液,静置,取上层清液,再滴加FeCl3溶液
(1)化学是一门以实验为基础的科学。根据如图图示回答问题。
①仪器a的名称是 。
②实验室用高锰酸钾制取氧气的化学反应方程式为 。所选用的发生装置是 (填序号)。 若用E装置收集氧气,实验完毕后,先将导管从水槽中移出,再熄灭酒精灯的目的是 。
③氢气是一种清洁能源。实验室常用锌粒和稀硫酸来制取氢气,应选择的发生装置是 (填序号,下同),收集装置除选E外,还可以选 。
(2)化学小组同学设计了如图所示装置(夹持仪器已略去)做了2个趣味实验。实验时,打开止水夹,C瓶内的水流入D中,使B试管内气压减小,B中长导管口有气泡冒出。
①在A处烧杯内放置燃烧的蜡烛,打开止水夹,B中无色溶液变浑浊,B中的试剂是 。
②在A处烧杯内放置某溶液,打开止水夹。若B中盛有紫色石蕊溶液,石蕊溶液变红色;若B中盛有红色溶液,红色溶液变无色。则A处烧杯内的溶液是 ,B中红色溶液可能是 。
