某同学要探究燃烧的条件和空气中氧气的含量,进行了如下实验。
[实验一](已知:白磷的着火点为40℃)
实验装置 |
实验步骤及现象 |
|
步骤Ⅰ.检验装置的气密性,气密性良好。 步骤Ⅱ.将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧。 步骤Ⅲ.向A瓶中加满80℃热水,塞紧瓶塞,白磷不燃烧。 步骤Ⅳ.打开K1、K2,从a口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2.此时进入量筒B中水的体积为200mL,观察到A瓶中的白磷燃烧。 |
(1)对比步骤Ⅱ和Ⅳ的现象可知,可燃物燃烧的条件之一是
(2)待装置冷却一段时间后,打开K2,如果观察到 ,说明空气中氧气的体积约占 .若实验测得空气中氧气的体积分数小于
.若实验测得空气中氧气的体积分数小于 ,原因可能是 (答一条即可)。
,原因可能是 (答一条即可)。
[实验二]用如图所示装置,利用铁生锈的原理也可以比较准确地测出空气中氧气的含量。若将此装置中的细铁丝换成足量的细铜丝进行实验,能否比较准确地测出空气中氧气的含量,并说明理由 。[已知:铜能与空气中氧气、水、二氧化碳反应生成铜绿。化学方程式:2Cu+O2+H2O+CO2═Cu2(OH)2CO3]

某班学生分三组分别做了二氧化碳制取和性质验证实验,如图所示。实验结束后,老师取两份等质量的丙废液,分别与甲、乙废液混合,将甲废液与丙废液倒入烧杯A中,有白色沉淀生成;将乙废液与丙废液倒入烧杯B中,有气泡产生。请填空:
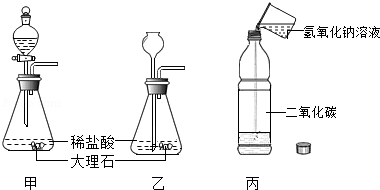
(1)甲废液与乙废液所含溶质的成分可能不同的是 (用化学式填空,下同)
(2)烧杯A中沉淀的成分一定有 。
(3)另取少量丙废液样品,加入足量的氯化钡溶液,有白色沉淀生成,过滤,向滤液中滴加氯化铁溶液,观察到有红褐色沉淀生成,未发现其他明显现象。由此推测出,丙废液溶质的成分是 ,丙废液与氯化钡溶液反应的化学方程式为 ,烧杯A的上层清液中溶质的成分一定有 。
实验是进行科学探究的重要方式,某同学设计如图所示实验,探究二氧化碳的有关性质。请填空:
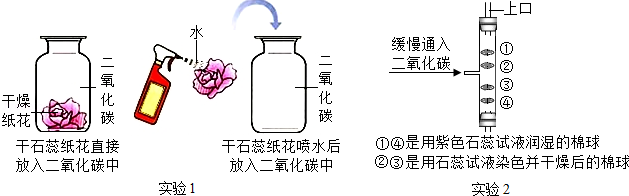
(1)实验1采用科学探究中的控制变量法,该实验控制的变量是 。
(2)实验1中干石蕊纸花喷水后放入二氧化碳中,观察到的现象是 ,该反应的化学方程式是 。
(3)实验2是在实验1的基础上设计的创新改进实验,将二氧化碳缓慢通入竖直放置的玻璃管中,能观察到第 (填序号)号棉球先变色,通过此现象可获得关于二氧化碳的另外一条性质是 。
元素的性质与原子结构密切相关,请填空:
(1)氟元素(F)的原子结构示意图如图所示,据图可判断出x的数值为 ;氟原子在化学反应中易 电子(填“得”或“失”),所以氟元素在化合物中的化合价通常为 价.
(2)氢元素与氟元素形成的化合物为氟化氢,其化学式为 2)是一种气体,能与水反应生成氟化氢和氧气,此反应的化学方程式为 .
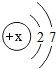
酸奶是日常生活中常见的一种食品,如表是某酸奶外包装上标识的营养成分表.
|
项目 |
能量 |
蛋白质 |
脂肪 |
糖类 |
钠 |
|
每100g |
329kJ |
2.6g |
3.1g |
10.0g |
60mg |
请填写下列空格:
(1)酸奶中的 在消化道内会逐渐被分解成可被人体吸收的多种氨基酸.
(2)脂肪在人体内分解、氧化释放出能量的过程,是将 能转化为热能.
122211)是酸奶中的一种糖类物质,蔗糖的组成中碳、氢元素的质量比为(最简整数比) .
(4)在选择制作酸奶包装盒的材料时,从化学性质的角度分析该材料应具备 的特点(填写一条即可)
根据下列装置,回答问题:

(1)写出图中标号仪器的名称:① ;② .
(2)实验室用过氧化氢溶液和二氧化锰制取氧气时,发生反应的化学方程式为 ,从控制反应速率和节约药品的角度考虑,发生装置最好选用 (填装置序号).
(3)因为氧气不易溶于水,所以可以利用装置 (填装置序号)收集,如果要做铁丝在氧气中燃烧的实验,用这种装置收集氧气时应注意 .