甲、乙两个化工厂的废液中共含有硫酸铜、硫酸、碳酸钠和氢氧化钠四种溶质,每个厂各含其中两种。某校社会实践小组的同学对两个厂的废液成分进行探究。
(1)取甲厂的废液观察,废液呈蓝色,结合溶液中物质共存的原理可推知,甲厂废液中的溶质是 ,将所取废液部分倒入试管中并加入足量锌片,观察到的实验现象是 。
(2)同学们设计以下实验对乙厂废液中的成分进行了验证。
实验步骤 |
实验现象 |
实验结论 |
实验一:取少量乙厂废液于试管中,滴入足量Ba(NO3)2溶液 |
产生白色沉淀 |
乙厂废液中含有 |
实验二:取实验一试管中的上层清液,滴入 |
|
①请写出实验一中发生反应的化学方程式 。
②下列物质可以代替实验一中Ba(NO3)2溶液的是 。
A.稀盐酸 B.氢氧化钡溶液
C.氯化钡溶液 D.氢氧化钙溶液
如图是实验室用于气体制备的装置,请根据图示回答问题:
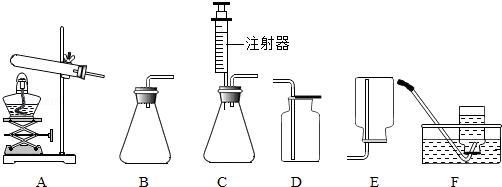
(1)实验室用氯酸钾制取氧气应选择的发生装置是 (填序号,下同).
(2)实验室中能用于过氧化氢溶液制氧气,且便于随时添加液体药品的发生装置是 ;要想得到比较纯净的氧气,需选择的收集装置是 .
(3)实验室制取二氧化碳时,应选择的收集装置是 ,理由是 ;判断CO 2是否收集满的方法是 .
实验室有一瓶标签模糊的烧碱溶液,小杰设计实验测定了其溶质质量分数.请根据如图所示的实验过程和提供的数据进行分析和计算.(注:滴入酚酞试液的质量忽略不计)
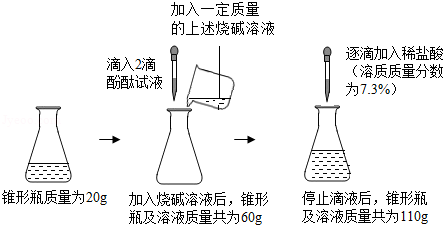
(1)将稀盐酸逐滴滴入锥形瓶的过程中,应边滴加边摇动锥形瓶,当观察到溶液颜色恰好 时,停止滴液,反应所消耗稀盐酸的质量为 g.
(2)通过计算确定该瓶烧碱溶液的溶质质量分数.(写出计算步骤)
(3)问题讨论:小红做同样的实验得到的结果比小杰得到的结果偏小,从实验操作的角度分析产生这种误差的原因可能是 (填写一条即可)
元素的性质与原子结构密切相关,请填空:
(1)氟元素(F)的原子结构示意图如图所示,据图可判断出x的数值为 ;氟原子在化学反应中易 电子(填"得"或"失"),所以氟元素在化合物中的化合价通常为 价.
(2)氢元素与氟元素形成的化合物为氟化氢,其化学式为 ;常温下,氟气(F 2)是一种气体,能与水反应生成氟化氢和氧气,此反应的化学方程式为 .
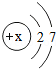
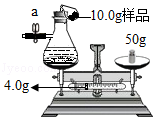
某化学课外活动小组测定长期放置的铁粉中铁单质的百分含量.他们准确称量两份质量各为10.0g的铁粉样品,分别进行如下操作:
(1)如图所示甲同学记录天平砝码和游码的数据为54.0g.将气球中的10.0g铁粉样品加入到盛有过量的稀硫酸的锥形瓶中,反应停止后,天平是否平衡(不考虑空气浮力) (填"是"或"否");要想获取实验的相关数据,后面必须的操作是 (假设气球不破裂且能恢复原状).
| A. |
打开弹簧夹a放出气体 |
B. |
取下砝码 |
| C. |
向右拨动游码至天平平衡 |
D. |
向左拨动游码至天平平衡 |
(2)乙同学把10.0g铁粉样品加入到足量的硫酸铜溶液中,充分反应后过滤、洗涤、干燥、称量,得到固体10.8g,计算该样品中铁单质的百分含量.(写出计算过程)
实验室开放日,化学小组的同学来到实验室,对酸的性质很感兴趣,向老师提出研究硝酸的性质,老师高兴答应并带领同学们进行了硝酸性质的实验探究。
[实验设计]
(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变 色;
(2)将Zn片投入稀硝酸中,预计将产生氢气。
[实验验证]同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B。
[提出问题]
(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?硝酸具有哪些特性?
[查阅资料]看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成H2。
(2)含氮元素的某些气态物质的物理性质
|
NH3 |
N2 |
NO |
NO2 |
|
|
颜色 |
无色 |
无色 |
无色 |
红棕色 |
|
溶解性 |
极易溶于水 |
不溶于水 |
不溶于水 |
可溶于水或硝酸 |
[猜想与分析]
(1)小明同学认为石蕊变色后又褪色的原因是由于试管不干净,含有其他杂质造成的,要证明小明的观点,应进行的操作是
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①小丽同学认为A是NH3,但遭到了大家的一致反对,原因是 ;
②小强同学认为A是N2,也遭到大家的一致反对,原因是 ;
③经讨论,最终大家获得了A是NO,NO在试管口遇氧气生成NO2的共识。
[实验探究]小红同学对硝酸与Cu反应很感兴趣,便取了一小块Cu片投入稀HNO3中,发现Cu片溶解,也出现了上述Zn与稀HNO3反应的类似现象,确认生成了NO,并在老师的帮助下,测出恰好反应的Cu和HNO3的质量比为8:21,由此获得了Cu与稀HNO3的反应化学方程式 。
[交流与反思]根据探究结果,请你解释稀HCl跟Cu不反应而稀HNO3却能跟Cu反应的原因 。