高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。某工厂以22.35 kg NaClO固体、若干Fe2(SO4)3固体和质量分数为20%的NaOH溶液为原料生产Na2FeO4,反应原理为:3NaClO+Fe2(SO4)3+10NaOH═2Na2FeO4+3NaCl+3Na2SO4+5H2O,假设反应物均恰好完全反应。试计算:
[已知:相对分子质量为NaClO 74.5 Fe2(SO4)3 400 Na2FeO4 166]
(1)Na2FeO4中质量分数最大的元素是 。
(2)制备过程中需加入20%的NaOH溶液的质量是多少?
(3)最后所得溶液中Na2FeO4的质量分数是多少?(计算结果精确到0.1%)
侯德榜是我国著名的化学家,发明了侯氏制碱法,其反应原理如下:NaCl+CO 2+NH 3+H 2O═NaHCO 3+NH 4Cl,请计算:
(1)氯化铵中氮元素的质量分数。
(2)生产8.4t碳酸氢钠,理论上需要氯化钠的质量。
尿素[CO(NH 2) 2]是一种常见的氮肥,工业上制备反应如下:
CO 2+2NH 3 CO(NH 2) 2+H 2O,请计算:
(1)尿素中氮元素的质量分数。
(2)生产6t尿素,理论上需要氨气的质量是多少?
实验室加热氯酸钾(KClO 3)和二氧化锰的混合物28.0g制取氧气,完全反应后剩余固体质量为18.4g,请计算:
(1)生成氧气的质量。
(2)原混合物中氯酸钾的质量。
早在西汉时期的《淮南万毕术》中就记载"曾青得铁则化为铜",成为现代湿法冶金的先驱。现有含1.6kg硫酸铜的工业废液,加入铁粉回收铜,请计算:
(1)硫酸铜中铜元素的质量分数。
(2)理论上与硫酸铜反应消耗铁粉的质量。
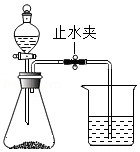
海螵蛸是一味中药,其主要成分是碳酸钙,某同学利用如图装置测定其中碳酸钙的含量。
①在锥形瓶中加入质量为m的海螵蛸粉末,向分液漏斗中加入稀盐酸。在烧杯中加入足量氢氧化钠溶液,并称量烧杯及氢氧化钠溶液总质量m 1。
②先打开止水夹,再打开分液漏斗活塞,滴加盐酸并及时关闭活塞。完全反应后,再次称量烧杯及其中液体的总质量m 2。
③利用m 2与m 1的差值,计算反应生成的二氧化碳质量,再计算海螵蛸中碳酸钙的含量。
(1)海螵蛸具有治疗胃酸过多、能为骨质发育提供重要元素的功效,其原因是 。
(2)实验前要检查装置的气密性,方法是:用止水夹夹住橡胶管,往分液漏斗中加入适量水。打开分液漏斗的活塞,观察到 ,说明装置气密性良好。
(3)下列情况会导致海螵蛸中碳酸钙质量分数测量值偏小的是 (可多选)。
A.海螵蛸中滴加盐酸过量
B,锥形瓶内部分水蒸气随二氧化碳逸出
C.反应结束后,锥形瓶内有二氧化碳残留
D.反应速度过快,大量气泡从氢氧化钠溶液中溢出