镁元素广泛应用于火箭、导弹和飞机制造业,被称为“国防元素”。如图1所示为制取单质镁的转化过程,试回答下列问题:
如图转化过程中发生的化学反应主要有:

MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl═MgCl2+2H2O,MgCl2 Mg+Cl2↑
(1)在过程①中,所加石灰乳的主要成分是 (填写化学式)。
(2)过程②所发生的反应属于 (填“化合”“分解”“置换”或“复分解”)反应。
(3)下列有关过程③中能量转化的说法,正确的是 (填选项序号)。
A.电能转化为化学能 B.化学能转化为电能 C.潮汐能转化为化学能
(4)海水或卤水中本来就含有氯化镁,还需要过程①②的原因是 (选项序号)。
A.将氯化镁富集提纯 B.生成更多氯化镁 C.使石灰乳和稀盐酸反应
(5)某化学兴趣小组欲测定某氯化镁样品中MgCl2的含量(杂质为NaCl),称取10g该样品将其置于干净的烧杯中,加入适量水,使固体样品完全溶解。向所得溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与滴入NaOH溶液的质量关系如图所示。试回答下列问题:

①当滴入NaOH溶液120g时(即图中B点),烧杯中溶液里含有的溶质为 (写化学式)。
②当滴入10%的NaOH溶液80g时(即图中A点),恰好完全反应,试通过计算,求10g此氯化镁样品中MgCl2的质量。(计算结果精确至0.1g)
中和反应在日常生活中应用广泛,下列是稀盐酸和氢氧化钠溶液反应的微观示意图。回答以下问题: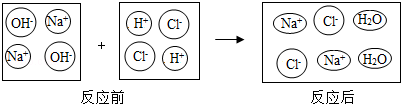
(1)分析图中反应前后没有发生变化的微粒是 、 ;反应的实质是 。
(2)如果规定上述反应后溶液的pH<7,显酸性。请你设计一个实验方案证明溶液显酸性:
|
实验操作 |
实验现象 |
实验结论 |
|
①
|
②
|
显酸性 |
2017年5月,我国在南海海域成功开采可燃冰。可燃冰外观像冰,主要成份是甲烷水合物(甲烷分子和水分子组成),可表示为 CH4•nH2O,在开采过程中,若甲烷泄漏会导致严重的温室效应。
某化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计实验探究:
[提出问题]甲烷燃烧后生成哪些物质?
[查阅资料]①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;
②白色无水CuSO4粉末遇水变蓝色;
③CO与人体内的血红蛋白结合,会造成人中毒缺氧。
[猜想与假设]猜想一:CO2、H2O. 猜想二:CO、H2O;猜想三:CO2、CO、H2O
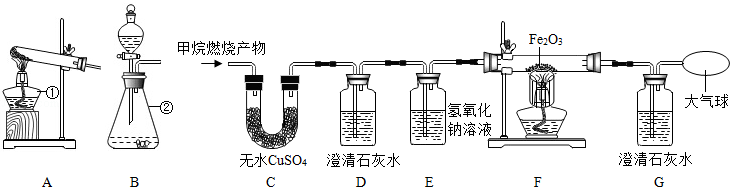
[实验探究]将甲烷在一定量的纯净氧气中燃烧的产物依次通过C﹣G装置(部分夹持、固定装置省略)进行验证:
(1)装置A、B中标有数字的仪器名称 ① ,② 。
若选用过氧化氢溶液和二氧化锰来制取氧气,应选用的发生装置是 ;该反应的化学方程式为 ;
(2)实验过程中观察到C中白色粉末变为蓝色,D、G中澄清石灰水变浑浊,F中红色粉末变成黑色,由此推断猜想 成立。
(3)实验过程中D装置的作用是 ;该反应的化学方程式是 。
(4)实验过程中用纯净O2而不用空气的原因是 。
(5)实验过程中C、D装置的顺序不能颠倒,原因是 。
[反思与交流]日常生活中,使用含碳燃料一定要注意通风,防止 中毒。
AgNO3可用于电影胶片制作。现取含有NaNO3的AgNO3样品100g,在一定条件下让样品充分反应,只有AgNO3发生反应,得到固体69g,该过程中发生反应的化学方程式为:2AgNO3 2Ag+2NO2↑+O2↑.试计算:
2Ag+2NO2↑+O2↑.试计算:
(1)AgNO3中N、O元素的质量比为 。
(2)分解产生的混合气体中O2的质量。
(3)另取100该样品和一定质量的NaCl固体全部溶解于142.5g水中,得到含一种溶质的溶液,该溶液溶质的质量分数是多少?
Ca(OH)2变质得到Ca(OH)2和CaCO3的混合物。李琳同学设计了如图的实验装置来测定CaCO3的含量。她用气密性良好的装置装上药品并通一会儿N2后关闭止水夹,再打开分液漏斗活塞。提示:碱石灰(可以吸收CO2和H2O)、浓硫酸均足量,稀盐酸不考虑其挥发性。
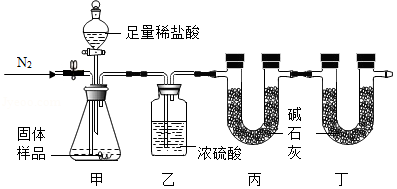
(1)通入N2的原因之一是N2的化学性质 (填“活泼”或“不活泼”)。
(2)甲装置中发生中和反应的化学方程式为 。
(3)浓硫酸的作用是 。
(4)测定CaCO3的含量需要测定两个物理量,其中一个物理量为样品的质量。
①另一个物理量为 (填序号)。
A.滴下的稀盐酸质量
B.反应前后乙装置增加的质量
C.反应前后丙装置增加的质量
D.反应前后丁装置增加的质量
②若去掉丁装置,测得CaCO3含量 (填“偏高”、“偏低”或“不变”)。
③甲装置中反应结束后打开止水夹再通入一会儿N2的目的是 。
氧气在中学化学中有着举足轻重的地位。

(1)实验Ⅰ中仪器①的名称为 ,现象为铁丝剧烈燃烧,火星四射,产生 色固体。
(2)实验Ⅱ为电解水制氧气,发生反应的化学方程式为 。气体a在电源的 (填“正”或“负”)极端产生。
(3)实验Ⅲ为测定空气中氧气含量的实验,在瓶内加入少量水、并将水面上方空间分为5等份,接下来的实验步骤依次为 (填序号),最后打开弹簧夹。
①冷却到室温
②弹簧夹夹紧橡皮管
③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧