冬季雾霾频发,某校社会实践小组的同学们,对某地区雾霾的成分、成因、危害及防治产生了浓厚的兴趣并开启了项目性学习之旅。
[信息检索]雾是浮游在空中的大量微小水滴。霾是可吸入颗粒物浓度较高造成的能见度较低的现象。霾的主要成分可能含有可溶性硫酸盐、硝酸盐,铵盐、不溶性有机物、黑碳、金属元素和其它元素。
[提出问题]某地霾的成分是什么?
[实验准备]选择该地重度雾霾天气,用SDLKC﹣1000型大流量TSP采样器在室外采集大气中的可吸入颗粒物10g。
活动一:探究霾中是否含有铵盐和硫酸盐。
实验方案 |
实验步骤 |
实验现象 |
实验结论 |
方案一 |
取5g样品,加少量熟石灰末,混合、研磨 |
|
含有铵盐 |
方案二 |
取5g样品,加适量水,充分溶解后过滤,向滤液中滴加 |
有白色沉淀生成 |
含有硫酸盐 |
[总结反思]工业上应加强对污染企业的监管,农业上应合理施用化肥。
活动二:探究霾中是否含有黑碳。同学们设计了如图所示的创新实验。(将活动一得到的残渣,干燥后置于中间凹槽内)
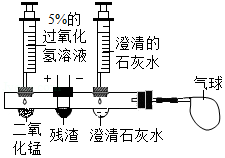
[实验步骤]①滴入过氧化氢溶液制取O2,排出装置内空气后,再在导管口接上气球。
②向右边的凹槽内滴入澄清的石灰水,
③接通电源,用热电阻丝点燃残渣
[实验现象]残渣剧烈燃烧,澄清石灰水浑浊,气球变大。
[实验结论]霾中含有黑碳。装置内澄清石灰水变浑浊的化学方程式是 。
[交流研讨]某同学对“霾中含有黑碳”的结论产生质疑,理由是 。
活动三:查阅资料,霾中还含有Al、Na、Zn、Pb、Hg、Cd等金属元素,其中的有害元素除Cd外,还有 。
[能力发展]请你联系实际填写关于雾霾的问卷调查表:
项目 |
雾霾频发的成因 |
控制雾霾频发的做法 |
政府采取的应急措施 |
① |
能源结构不同 |
推广太阳能发电 |
人工降雨 |
② |
烧散煤取暖 |
|
向空中或地面洒水 |
③ |
|
推广新能源汽车 |
私家车限号出行 |
[检出进度]小组同学没有进行的探究项目是 。
金属及其化合物在生产生活中有广泛的应用。

(一)金属的应用和防护
(1)用不锈钢、合成橡胶、氧化镁等材料制造的飞机轮胎属于 材料。
(2)航空煤油是飞机的燃料,它主要是由 炼制的。
(3)铁易生锈,提出防止铁生锈的一种方法 。
(4)特种钢中含有少量Mn、MnO2和Al粉混合在高温下反应可得到Mn,该反应的化学方程式为 。
(5)Mg(OH)2受热分解生成高熔点的MgO.Mg(OH)2可用作阻燃剂,其主要原理是 (选填序号)。
a.分解吸热,降低可燃物着火点 b.MgO覆盖燃烧物,隔绝氧气
(二)制备还原性铁粉
实验室利用废铁屑(含少量Fe2O3)为原料制备还原性铁粉的流程如下:
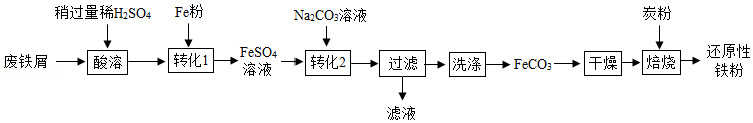
(1)Fe粉可使“酸溶”产生的Fe2(SO4)3转化为FeSO4,该反应的化学方程式为 。
(2)检验FeCO3已洗净的方法:取最后一次洗涤后的滤液,先加入一定量稀盐酸,再滴加 溶液,无明显现象。
(3)“干燥”时有少量FeCO3发生下列转化:FeCO3 FeOOH+CO2,该转化的化学方程式为 。
(4)“焙烧”前,应将炭粉与“干燥”所得固体均匀混合,目的是 。
(三)测定还原性铁粉的组成
还原性铁粉中含有少量FexCy,小组同学在老师的指导下进行以下实验。
资料:①Fe,FexCy在加热时与O2反应能生成相应氧化物。
②FexCy不与酸反应。
实验1:取29.52g样品,加入足量稀H2SO4,充分反应后生成1.00gH2。
实验2:另取29.52g样品,按如图进行实验。

表:装置A和B的质量变化
|
装置 |
A |
B |
|
反应前 |
300.00 |
400.00 |
|
反应后 |
m |
400.44 |
实验后A中固体全部变为红棕色,装置A、B的质量变化如上表。
(1)装配好装置后,实验前先要 。
(2)装置C的作用是 。
(3)FexCy中,x:y= 。表中m的值是 。
反思:若用空气替代O2进行实验,测得x:y的值偏大,可能的原因是 。
如图为某些物质间的转化关系(部分反应条件省略)。A、B、E、F、G均为气体,B能使稀高锰酸钾溶液褪色,E、F组成元素相同,且F有毒,G是一种最轻的气体;乙、丁均为黑色的固体氧化物,反应④是工业炼铁的原理;反应②是光合作用。

(1)化学式:G ,丙 。
(2)反应①、④的化学方程式:① ;④ 。
(3)甲一定含有的元素是 。
(4)Fe与蓝色溶液的反应属于 反应(填基本反应类型)。
现有一包固体粉末,可能含有K2SO4,CuSO4,NaOH,BaCl2,Mg(NO3)2,BaCO3中的一种或几种。进行如下实验:
(1)取少量固体溶于足量水中,过滤得到白色固体A和无色滤液B,则原固体中一定不含有 。
(2)向固体A中加入足量稀盐酸,固体全部溶解,无气泡产生,则原固体中一定含有 一定不含有 。
(3)向滤液B中通入CO2,产生白色沉淀,则原固体中一定还含有 ,一定不含有 。
草酸(H2C2O4)是一种酸,易溶于水。
(一)草酸的化学性质
(1)草酸溶液的pH 7(选填“>”“<”或“=”)。
(2)草酸溶液中加入石灰水,生成草酸钙(CaC2O4)固体,该反应的化学方程式为 。
(二)CaC2O4热分解探究
资料:CaC2O4 CaCO3+CO↑
兴趣小组称一定量的CaC2O4固体,在老师的指导下用如图装置进行实验。
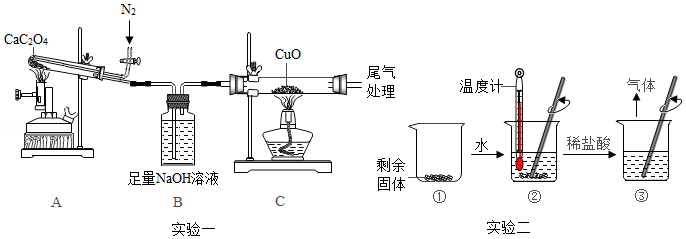
实验一:先通入N2,再加热相应固体,一段时间后停止加热,缓缓通入N2至试管冷却。
(1)装置B增重6.6g,装置B中发生反应的化学方程式为 。
(2)装置C中观察到 的现象,说明反应生成CO。
实验二:取出实验一后装置A试管中的剩余固体,按图①﹣③进行实验。
(3)②中温度升高,则剩余固体中含有 ,③中产生2.2g气体。
(4)将③中溶液蒸发得CaCl2固体22.2g。
结论:(1)取用的CaC2O4固体的质量为 g。
(2)本实验中CaC2O4分解的总反应化学方程式为 。
请结合如图回答问题:
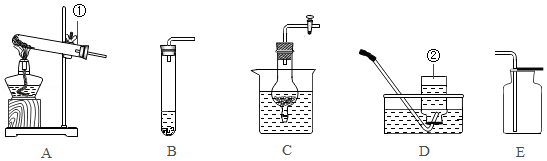
(1)仪器名称:① ,② 。
(2)实验室用氯酸钾和二氧化锰制取并收集O2,可选用发生装置 (选填序号)和收集装置D组合,反应的化学方程式为 。
(3)实验室制取CO2的化学方程式为 ,用装置C相对于B的优点是 ,CO2可用装置E收集,理由是 。
(4)实验室用FeS和稀H2SO4反应制取H2S.H2S是有毒气体,能溶于水,其水溶液为氢硫酸。
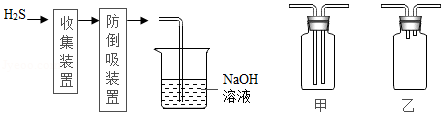
①制取H2S的化学方程式为 。
②图中“防倒吸装置”应选择 (选填“甲”或“乙”)
③NaOH溶液的作用是 。